
Wetenschap
Chloorreactiviteit:chemische reacties en verbindingen begrijpen
* Hoge elektronegativiteit: Chloor heeft een hoge elektronegativiteit, wat betekent dat het sterk elektronen aantrekt. Dit maakt het gretig om een elektron te verkrijgen om een stabiele elektronenconfiguratie te bereiken.
* Zeven Valentie-elektronen: Chloor heeft zeven elektronen in de buitenste schil. Het heeft nog maar één elektron nodig om een volledig octet te bereiken, waardoor het zeer reactief is.
Voorbeelden van chloorreacties:
* Metalen: Chloor reageert gemakkelijk met de meeste metalen en vormt metaalchloriden. Natrium reageert bijvoorbeeld heftig met chloorgas en vormt natriumchloride (NaCl), een gewoon keukenzout.
* Niet-metalen: Chloor reageert ook met veel niet-metalen. Het reageert bijvoorbeeld met waterstof en vormt waterstofchloride (HCl), een sterk zuur.
* Organische verbindingen: Chloor reageert met organische verbindingen en vormt gechloreerde verbindingen. Dit wordt gebruikt bij de productie van kunststoffen, pesticiden en farmaceutische producten.
Opmerking: Chloorreacties kunnen zeer exotherm zijn, wat betekent dat er veel warmte vrijkomt. Sommige reacties kunnen explosief of gevaarlijk zijn. Het is belangrijk om voorzichtig met chloor om te gaan.
 Onderzoekers werpen licht op hoe fotopolymerisatie veel efficiënter kan worden gemaakt
Onderzoekers werpen licht op hoe fotopolymerisatie veel efficiënter kan worden gemaakt  Wat is het beste instrument om een oplossing voor te bereiden?
Wat is het beste instrument om een oplossing voor te bereiden?  Wat te doen tegen zwavelverbranding op het gezicht?
Wat te doen tegen zwavelverbranding op het gezicht?  Wat is het product van een bèta-emissie van Strontium-90?
Wat is het product van een bèta-emissie van Strontium-90?  Wat is de kleur van kaliumbromide opgelost in water?
Wat is de kleur van kaliumbromide opgelost in water?
 Papier weggooien zodat het kan worden gerecycled
Papier weggooien zodat het kan worden gerecycled  NO2– niet zo erg als we dachten?
NO2– niet zo erg als we dachten? Bosbranden in mediterrane bossen aanpakken
Bosbranden in mediterrane bossen aanpakken bossen, koolstofputten, kan vertragingen bij het koolstofarm maken van de economie niet goedmaken:studie
bossen, koolstofputten, kan vertragingen bij het koolstofarm maken van de economie niet goedmaken:studie Hoe beïnvloeden biotische en abiotische factoren de ecosysteemfunctie van de gemeenschapsstructuur?
Hoe beïnvloeden biotische en abiotische factoren de ecosysteemfunctie van de gemeenschapsstructuur?
Hoofdlijnen
- Celgroei en organismegrootte:hoe beïnvloedt de grootte de celproductie?
- Welke biotische factoren hebben Red Wolf?
- Het overbruggen van twee veelvraatpopulaties in Fennoscandia is noodzakelijk voor het behoud
- Wat zijn analogieën voor lysosomen?
- Welk type cellen bevatten een kern?
- De theorie van de biogenese stelt dat?
- Hoe heet het als een organisme met twee allelen hetzelfde is?
- Haploïde gameten:het chromosomenaantal bij seksuele voortplanting begrijpen
- Wat is in de eerste plaats verantwoordelijk voor cytokinese in plantencellen?
- Onderzoekers vorderen inspanningen om glyfosaatpesticide in haver nauwkeurig te meten

- Nieuwe sensor om atmosferische aerosolen en stikstofdioxide tegelijkertijd te meten
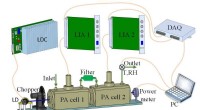
- Nieuwe hout-metaalhybride voor lichtgewicht constructie

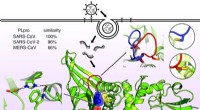
- Informatie over de moleculaire vorm van virussen die COVID-19 veroorzaken, SARS, en MERS onthult structurele overeenkomsten
- De deuren openen naar effectieve COVID-19-behandelingen
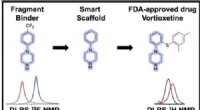
 Wat is Helm Glacier?
Wat is Helm Glacier?  Helium is essentieel voor onderzoek en medische apparatuur, maar het is niet hernieuwbaar en moeilijk te recyclen
Helium is essentieel voor onderzoek en medische apparatuur, maar het is niet hernieuwbaar en moeilijk te recyclen  Een gas oefent een druk uit van 0,892 atm in 5,00 L container bij 15 graden Celsius de dichtheid is 1,22 GL Welk molecuulgewichtgas?
Een gas oefent een druk uit van 0,892 atm in 5,00 L container bij 15 graden Celsius de dichtheid is 1,22 GL Welk molecuulgewichtgas?  Wat beweegt water tussen het aardoppervlak en de atmosfeer weer terug?
Wat beweegt water tussen het aardoppervlak en de atmosfeer weer terug?  Het buitengewone systeem voor het verzamelen van monsters van NASA's Perseverance Mars-rover
Het buitengewone systeem voor het verzamelen van monsters van NASA's Perseverance Mars-rover Soorten lood en hun voorbeeld?
Soorten lood en hun voorbeeld?  Staat de wet van behoud dat de totale hoeveelheid energie in het universum altijd hetzelfde is?
Staat de wet van behoud dat de totale hoeveelheid energie in het universum altijd hetzelfde is?  Het oudste gesteente van de aarde is mogelijk ontdekt (op de maan!)
Het oudste gesteente van de aarde is mogelijk ontdekt (op de maan!)
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

