
Wetenschap
Chemische coëfficiënten begrijpen:stoichiometrie uitgelegd
Hier is een overzicht:
* Wat het vertegenwoordigt: De coëfficiënt vertelt je de stoichiometrische verhouding van de reactanten en producten. Deze verhouding vertegenwoordigt het minimale aantal moleculen (of mol) dat nodig is om de reactie te laten plaatsvinden zoals geschreven.
* Hoe het werkt: In de vergelijking bijvoorbeeld:
```
2 H₂ + O₂ → 2 H₂O
```
* De coëfficiënt 2 voor H₂ betekent dat er twee mol waterstofgas (H₂) nodig is voor de reactie.
* De coëfficiënt 1 (impliciet) voor O₂ betekent dat er één mol zuurstofgas (O₂) nodig is.
* De coëfficiënt 2 voor H₂O geeft aan dat er twee mol water (H₂O) wordt geproduceerd.
Belangrijke opmerkingen:
* Coëfficiënten zijn hele getallen alleen. Je kunt geen breuken als coëfficiënten hebben in een uitgebalanceerde chemische vergelijking.
* Ze kunnen aangepast zijn om de chemische vergelijking in evenwicht te brengen, waarbij ervoor wordt gezorgd dat het aantal atomen van elk element aan beide zijden van de vergelijking gelijk is.
* Coëfficiënten veranderen niet de chemische formules van de reactanten of producten. Ze geven alleen de relatieve hoeveelheden aan van elke stof die bij de reactie betrokken is.
Het begrijpen van coëfficiënten is cruciaal voor:
* Voorspellen van de hoeveelheid reactanten en producten betrokken bij een reactie.
* Opbrengsten berekenen van producten in chemische reacties.
* Bepalen van de beperkende reactant bij een reactie.
Door coëfficiënten aan te passen om een chemische vergelijking in evenwicht te brengen, zorgen we ervoor dat de wet van behoud van massa wordt nageleefd, die stelt dat materie niet kan worden gecreëerd of vernietigd in een chemische reactie.
 Waarom beschouw je de gasvormige toestand van water als dampen terwijl dat ammoniakgas?
Waarom beschouw je de gasvormige toestand van water als dampen terwijl dat ammoniakgas?  Volgens welk basisprincipe wordt gefractioneerde destillatie toegepast bij het scheiden van mengsels?
Volgens welk basisprincipe wordt gefractioneerde destillatie toegepast bij het scheiden van mengsels?  Wat is het monomeer van koolhydraten?
Wat is het monomeer van koolhydraten?  Wat is een broos metaalelement met 4 letters?
Wat is een broos metaalelement met 4 letters?  Wat is er betrokken bij een chemische reactie?
Wat is er betrokken bij een chemische reactie?
Hoofdlijnen
- Wat is de functie van evolutie?
- Hoe verschillen de producten van gisting bij dieren van gist?
- Welke organel maakt protien?
- Chromosomen versus los DNA:de voordelen begrijpen
- Hoe stikstofbasen de genetische code vormgeven:een duidelijke gids
- Kuikenembryo's leveren waardevolle genetische gegevens voor het begrijpen van de menselijke ontwikkeling
- Onderzoek laat zien hoe beschadigde celkernen zichzelf opnieuw afsluiten en repareren
- Wat zijn de namen van cellen in STEM?
- Een 3D-model van een plantencel bouwen
- Schimmel als geluidsabsorbeerder

- HDPE-kunststof uitgelegd:gebruik, identificatie en voordelen

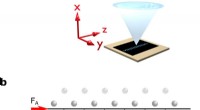
- Lasergekoelde ionen dragen bij aan een beter begrip van wrijving
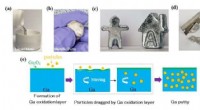
- Putty-achtige composieten van galliummetaal met potentieel voor toepassing in de echte wereld
- Onderzoek naar de elektronische neus voor het bewaken van de luchtkwaliteit, diagnose van ziekte

 Instagram rolt nieuwe functies uit om pesten tegen te gaan met AI
Instagram rolt nieuwe functies uit om pesten tegen te gaan met AI Een multishot lensloze camera in ontwikkeling kan helpen bij de diagnose van ziekten
Een multishot lensloze camera in ontwikkeling kan helpen bij de diagnose van ziekten Hoe werkt de wet van behoudsmassa en hoe verhoudt deze zich tot chemische vergelijkingen?
Hoe werkt de wet van behoudsmassa en hoe verhoudt deze zich tot chemische vergelijkingen?  Alle dieren hebben dit gas nodig om energie te maken van voedsel?
Alle dieren hebben dit gas nodig om energie te maken van voedsel?  Hoe werkt mechanische energie?
Hoe werkt mechanische energie?  Wat is 31,8 Celsius omgezet in Fahrenheit?
Wat is 31,8 Celsius omgezet in Fahrenheit?  Wat is verspillende energie?
Wat is verspillende energie?  Zijn straaldiagrammen van toepassing op convergerende lenzen en divergeren?
Zijn straaldiagrammen van toepassing op convergerende lenzen en divergeren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

