
Wetenschap
Covalente versus ionische obligaties:een uitgebreide gids
Covalente obligaties en ionische obligaties:
Covalente obligaties:
* Formatie: Gevormd wanneer twee atomen delen elektronen om een stabiele elektronenconfiguratie te bereiken.
* Natuur: Niet-metaalatomen met een vergelijkbare elektronegativiteit delen elektronen en vormen een sterke binding.
* Eigenschappen:
* Komt meestal voor tussen twee niet-metaalatomen.
* Hoge smelt- en kookpunten.
* Slechte geleiders van elektriciteit.
* Kan polair of niet-polair zijn.
* Voorbeelden: Water (H₂O), Kooldioxide (CO₂), Methaan (CH₄)
Ionische bindingen:
* Formatie: Gevormd wanneer één atoom overgaat een elektron naar een ander atoom, waardoor tegengesteld geladen ionen ontstaan die vervolgens tot elkaar worden aangetrokken.
* Natuur: Komt voor tussen een metaalatoom (neiging om elektronen te verliezen) en een niet-metaalatoom (neiging om elektronen te winnen).
* Eigenschappen:
* Meestal voorkomend tussen een metaal en een niet-metaal.
* Hoge smelt- en kookpunten.
* Goede geleiders van elektriciteit wanneer opgelost in water of gesmolten.
* Vormt doorgaans kristallijne vaste stoffen.
* Voorbeelden: Natriumchloride (NaCl), Calciumoxide (CaO), Magnesiumfluoride (MgF₂)
Hier is een tabel met een samenvatting van de belangrijkste verschillen:
| Kenmerk | Covalente binding | Ionische binding |
|----------------|------------------------------|------------------------------------------|
| Formatie | Het delen van elektronen | Overdracht van elektronen |
| Betrokken atomen | Meestal twee niet-metalen | Metaal en niet-metaal |
| Elektronegativiteit | Soortgelijke elektronegativiteit | Zeer verschillende elektronegativiteit |
| Smelt-/kookpunt | Over het algemeen hoog | Hoog |
| Geleidbaarheid | Slecht, behalve grafiet | Goed opgelost of gesmolten |
| Structuur | Moleculen | Kristallijne vaste stoffen |
| Voorbeelden | Water, methaan, kooldioxide | Natriumchloride, calciumoxide, magnesiumfluoride |
Samenvattend: Zowel covalente als ionische bindingen zijn cruciaal voor het creëren van stabiele moleculen en verbindingen, maar ze verschillen in hun vorming, eigenschappen en de soorten atomen die erbij betrokken zijn. Het begrijpen van deze verschillen is cruciaal voor het begrijpen van de aard van chemische bindingen.
 Wat is dan een relatie tussen klimaat en locatie van soorten?
Wat is dan een relatie tussen klimaat en locatie van soorten?  Gevolgen van olieramp in wetland aan de kust
Gevolgen van olieramp in wetland aan de kust Studie vindt een verband tussen droogte en luchtkwaliteit in de westelijke wildernis
Studie vindt een verband tussen droogte en luchtkwaliteit in de westelijke wildernis Herculische inspanningen redden huizen terwijl branden in Australië woeden
Herculische inspanningen redden huizen terwijl branden in Australië woeden Een halve graad warmer betekent 30, 000 meer doden per jaar in stedelijk China:studie
Een halve graad warmer betekent 30, 000 meer doden per jaar in stedelijk China:studie
Hoofdlijnen
- Hoe veranderde de uitvinding van de microscoop manier waarop mensen ziekten begrepen?
- Genetische studie onthult seksgeheimen van schimmels werpt licht op candidiasis
- De gezondheid van larven van een Antarctische koudwaterkoraalsoort kan resistent zijn tegen opwarmend water
- De geleidbaarheid van zenuwcellen in het centrale zenuwstelsel
- Waarom moeten grote organismen multicellulair zijn?
- Hoe bacteriën bacteriofagen in vivo ontwijken
- De effecten van temperatuur op enzymactiviteit en biologie
- Wat regelt andere klieren en lichaamsgroei?
- Welke term verwijst naar een oorspronkelijk gemaakt type organisme?
- Nieuwe coating kan grote gevolgen hebben voor lithiumbatterijen
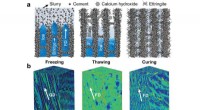
- Op hout geïnspireerd cement met hoge sterkte en multifunctionaliteit
- Hoe zuur bier zo... zuur wordt

- Drukken maakt polymeren plat, verbetering van elektrische en optische eigenschappen

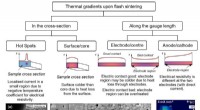
- Solid-state batterijen kunnen schoner worden gemaakt door flash-sintering op te schalen
 Wat zijn de drie meest voorkomende bacteriën die worden gebruikt voor het meten van de effectiviteit van een chemische stof?
Wat zijn de drie meest voorkomende bacteriën die worden gebruikt voor het meten van de effectiviteit van een chemische stof?  Welke planeet is de kleinste na Pluto?
Welke planeet is de kleinste na Pluto?  Wanneer zat in de plafondsterren glanzend gecreëerd?
Wanneer zat in de plafondsterren glanzend gecreëerd?  Waarom worden water en grond beschouwd als potentieel hernieuwbare energiebronnen?
Waarom worden water en grond beschouwd als potentieel hernieuwbare energiebronnen?  Fossiele schelpen onthullen zowel wereldwijde kwikverontreiniging als opwarming toen dinosauriërs stierven
Fossiele schelpen onthullen zowel wereldwijde kwikverontreiniging als opwarming toen dinosauriërs stierven Onderzoekers ontwikkelen nieuwe methoden om materialen op de kleinst mogelijke schaal te bestuderen
Onderzoekers ontwikkelen nieuwe methoden om materialen op de kleinst mogelijke schaal te bestuderen Ontcijferen hoe het lichaam de juiste opioïde enantiomeren kiest
Ontcijferen hoe het lichaam de juiste opioïde enantiomeren kiest  Robots trainen om chronische pijn te verlichten
Robots trainen om chronische pijn te verlichten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

