
Wetenschap
Covalente obligaties:de regel voor het verschil in elektronegativiteit begrijpen
De regel voor het verschil in elektronegativiteit van 0,4:
* Waar: Een verschil in elektronegativiteit van minder dan 0,4 resulteert waarschijnlijk in een niet-polaire covalente binding . Bij niet-polaire covalente bindingen worden elektronen gelijkelijk verdeeld tussen de atomen.
* Niet altijd nauwkeurig: Het elektronegativiteitsverschil alleen bepaalt niet altijd het type binding. Andere factoren zoals:
* De specifieke betrokken atomen: Zelfs met een klein verschil kan de aanwezigheid van zeer elektronegatieve atomen zoals zuurstof of fluor nog steeds resulteren in een enigszins polaire binding.
* De algemene moleculaire geometrie: Zelfs bij niet-polaire bindingen kan de vorm van het molecuul een dipoolmoment creëren, waardoor het in het algemeen polair wordt.
Belangrijke overwegingen:
* Polaire covalente obligaties: Elektronegativiteitsverschillen tussen 0,4 en 1,7 resulteren doorgaans in polaire covalente bindingen . Elektronen worden niet gelijk verdeeld, wat leidt tot gedeeltelijke positieve en negatieve ladingen op de atomen.
* Ionische bindingen: Elektronegativiteitsverschillen groter dan 1,7 leiden gewoonlijk tot ionische bindingen . Elektronen worden van het ene atoom naar het andere overgebracht, wat resulteert in geladen ionen die bij elkaar worden gehouden door elektrostatische krachten.
Samengevat:
Hoewel de 0,4-regel een nuttige richtlijn is, is het van cruciaal belang om te onthouden dat andere factoren bijdragen aan het type binding dat wordt gevormd. Het is het beste om elektronegativiteit te gebruiken als een van de vele hulpmiddelen voor het analyseren van bindingseigenschappen.
 Soorten natuurlijke bijenkorven
Soorten natuurlijke bijenkorven 11% kans op een nieuwe enorme aardbeving in Zuid-Californië, wetenschappers zeggen:
11% kans op een nieuwe enorme aardbeving in Zuid-Californië, wetenschappers zeggen: Stadstuinen stimuleren biodiversiteit, steden duurzamer maken
Stadstuinen stimuleren biodiversiteit, steden duurzamer maken Groenlands ijs is in de afgelopen miljoen jaar minstens één keer weggesmolten
Groenlands ijs is in de afgelopen miljoen jaar minstens één keer weggesmolten Giftige PAK-luchtverontreinigende stoffen uit fossiele brandstoffen vermenigvuldigen zich in zonlicht
Giftige PAK-luchtverontreinigende stoffen uit fossiele brandstoffen vermenigvuldigen zich in zonlicht
Hoofdlijnen
- Welke soorten organismen voeren de ademhaling uit?
- Hoe is DNA en de gelelektroforese -methode nuttig in de wetenschap?
- Is een muis eencellulair organisme?
- Hoe belangrijk is de oceaan voor het fotosyntheseproces?
- Wetenschappers vinden nieuwe conclusies over hoe sauropodeklauwen werden gebruikt
- Universeel klemeiwit stabiliseert gevouwen eiwitten:nieuw inzicht in hoe de chaperonne Hsp70 werkt
- Wat waren laden cellulair?
- Oud DNA brengt ons dichter bij het ontsluiten van de geheimen van hoe de moderne mens is geëvolueerd
- Wat is dit type weefsel dat onderdelen het lichaam maakt bewegen door te samentrekken of te verkorten?
- Geavanceerde polymeren helpen de waterzuivering te stroomlijnen, milieusanering

- De eerste ontdekking ter wereld kan de nieuwe groene ammoniakeconomie voeden

- Wetenschappers maken eerste biomoleculaire simulatie van miljarden atomen

- Onderzoekers ontdekken C-H-bindingsactiveringsreacties bij lage temperatuur door foto-geïnduceerde middelen
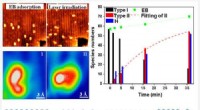
- De energieniveaus van organische halfgeleiders afstemmen

 Wat gebeurde er met de deeltjes in een thermometer wanneer de temperatuur daalt?
Wat gebeurde er met de deeltjes in een thermometer wanneer de temperatuur daalt?  Het deel van een atoom dat zich buiten de kern bevindt is _______.?
Het deel van een atoom dat zich buiten de kern bevindt is _______.?  Waarom kunnen bacteriën menselijke eiwitten produceren?
Waarom kunnen bacteriën menselijke eiwitten produceren?  Oude beenviskrachten heroverwegen hoe haaien evolueerden
Oude beenviskrachten heroverwegen hoe haaien evolueerden  Voormalige Audi-baas sluit zich aan bij ex-VW-chef in dok over dieselgate
Voormalige Audi-baas sluit zich aan bij ex-VW-chef in dok over dieselgate Nieuw onderzoek naar hoe overheden radicaal ecologisch en sociaal beleid kunnen financieren zonder bbp-groei
Nieuw onderzoek naar hoe overheden radicaal ecologisch en sociaal beleid kunnen financieren zonder bbp-groei  Een geoptimaliseerde structuur van memristive-apparaat voor neuromorfe computersystemen
Een geoptimaliseerde structuur van memristive-apparaat voor neuromorfe computersystemen Grumman EA-6B Prowler
Grumman EA-6B Prowler
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

