
Wetenschap
Natriumcarbonaat versus kaliumhydroxide:chemische tests voor differentiatie
1. Reactie met zuur:
* Natriumcarbonaat (Na₂CO₃): Reageert met verdunde zuren zoals zoutzuur (HCl) en produceert kooldioxidegas (CO₂), dat te herkennen is aan het bruisen en door het door kalkwater (calciumhydroxideoplossing) te leiden, dat melkachtig wordt.
```
Na₂CO₃ + 2HCl → 2NaCl + H₂O + CO₂
```
* Kaliumhydroxide (KOH): Reageert ook met verdunde zuren, maar produceert geen kooldioxidegas. In plaats daarvan vormt het een zout (bijvoorbeeld kaliumchloride, KCl) en water.
```
KOH + HCl → KCl + H₂O
```
2. Vlamtest:
* Natriumcarbonaat (Na₂CO₃): Wanneer het wordt verwarmd in de vlam van een bunsenbrander, produceert het een heldergele vlam. Dit komt door de aanwezigheid van natriumionen.
* Kaliumhydroxide (KOH): Produceert een lila of violette vlam bij verhitting in de vlam van een bunsenbrander, wat wijst op de aanwezigheid van kaliumionen.
3. Reactie met fenolftaleïne:
* Natriumcarbonaat (Na₂CO₃): Omdat het een zwakke base is, wordt de fenolftaleïne-oplossing roze.
* Kaliumhydroxide (KOH): Omdat het een sterke base is, zal het de fenolftaleïne-oplossing intenser roze of zelfs rood maken.
4. Neerslagtest:
* Natriumcarbonaat (Na₂CO₃): Bij reactie met bariumchloride (BaCl₂) vormt het een wit neerslag van bariumcarbonaat (BaCO₃).
```
Na₂CO₃ + BaCl₂ → BaCO₃↓ + 2NaCl
```
* Kaliumhydroxide (KOH): Vormt geen neerslag met bariumchloride.
Samengevat: Door deze chemische tests uit te voeren, kunt u effectief onderscheid maken tussen natriumcarbonaat en kaliumhydroxide.
 Chemici bereiken ongekende moleculaire drievoudige sprong met meerringige metaalcomplexen
Chemici bereiken ongekende moleculaire drievoudige sprong met meerringige metaalcomplexen Hoe planten cocaïne maken
Hoe planten cocaïne maken  Wat is de wetenschappelijke verklaring voor lagen vloeistoffen?
Wat is de wetenschappelijke verklaring voor lagen vloeistoffen?  Drie Halloween-wetenschapshacks om je griezelige seizoen naar een hoger niveau te tillen
Drie Halloween-wetenschapshacks om je griezelige seizoen naar een hoger niveau te tillen  Bedank de complexe chemie van gluten voor uw lichte, donzige bakproducten
Bedank de complexe chemie van gluten voor uw lichte, donzige bakproducten
 Verkenning van oceaanstromingen onder de Doomsday Glacier
Verkenning van oceaanstromingen onder de Doomsday Glacier Extreem winterweer, zoals Beest uit het Oosten, kan worden gekoppeld aan zonnecyclus
Extreem winterweer, zoals Beest uit het Oosten, kan worden gekoppeld aan zonnecyclus Klimaatscepticus of klimaatontkenner? Het is niet zo simpel
Klimaatscepticus of klimaatontkenner? Het is niet zo simpel Californië bosbrand fakkelt bos, dwingt nieuwe evacuaties af
Californië bosbrand fakkelt bos, dwingt nieuwe evacuaties af Het aanpassen van de CO2-uitstoot aan de verplichtingen van Parijs zou hittegerelateerde sterfgevallen voorkomen
Het aanpassen van de CO2-uitstoot aan de verplichtingen van Parijs zou hittegerelateerde sterfgevallen voorkomen
Hoofdlijnen
- Wat is de wetenschappelijke naam van evolutie?
- Welke biomen zijn er in Denemarken?
- Welk dier heeft scherpe tanden en evolueer het eten van vlees?
- Wat is de drie nucleotide?
- Beschrijf de ruggengraat van een RNA -molecuul?
- Welke plantengroep wordt gekenmerkt door dominante sporofyt vasculaire weefsels en zaden die op kegels worden blootgesteld?
- Wat is de biologische rol van maltose?
- Hoe hebben wetenschappers bepaald of het gedrag instinct of geleerd is?
- Wat is nucleaire pluse of?
- Minder zout, meer eiwit:aanpak van zuivelverwerking, milieu, duurzaamheidskwesties
- Het reactiequotiënt berekenen (Q):een praktische gids

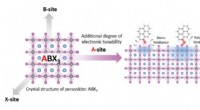
- Nieuwe manier om nanomaterialen krachtiger te maken voor elektronische toepassingen
- Zoutzuur versus zoutzuur:dezelfde stof, verschillende namen

- Onderzoekers ontwikkelen techniek om koolstofdioxide en methaan te hergebruiken

 Fix voor 737 MAX anti-stall software is klaar:industriebronnen (update)
Fix voor 737 MAX anti-stall software is klaar:industriebronnen (update) Waar gebruiken mensen zwavel voor?
Waar gebruiken mensen zwavel voor?  Wat is iets interessants aan Titanium?
Wat is iets interessants aan Titanium?  Wat is niet -instantie?
Wat is niet -instantie?  Het antropoceen begon in 1965, volgens tekens in 's werelds eenzaamste boom
Het antropoceen begon in 1965, volgens tekens in 's werelds eenzaamste boom Deskundigen waarschuwen voor hitterisico's nu de temperatuur in India weer stijgt
Deskundigen waarschuwen voor hitterisico's nu de temperatuur in India weer stijgt  Wat is een noodzakelijk product van de verbrandingsreactie?
Wat is een noodzakelijk product van de verbrandingsreactie?  Wat voor soort energie gebruikt een lift?
Wat voor soort energie gebruikt een lift?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

