
Wetenschap
Natriumacetaat versus zwavelzuur als katalysatoren:hun rol begrijpen
* Natriumacetaat (CH₃COONa):
* Wordt vaak gebruikt als basiskatalysator. Het wordt vaak gebruikt bij veresteringsreacties, waar het helpt de zure bijproducten te neutraliseren en de reactie vooruit te helpen.
* Voorbeeld: Bij de verestering van azijnzuur met ethanol werkt natriumacetaat als een basische katalysator om het geproduceerde water te verwijderen, waardoor het evenwicht in de richting van estervorming verschuift.
* Zwavelzuur (H₂SO₄):
* Vaak gebruikt als zure katalysator. Het wordt vaak gebruikt bij uitdrogingsreacties, waarbij het helpt watermoleculen uit reactanten te verwijderen.
* Voorbeeld: Bij de dehydratatie van ethanol om etheen te vormen, werkt zwavelzuur als een zure katalysator om de alcohol te protoneren, waardoor deze gevoeliger wordt voor waterverlies.
Het kiezen van de juiste katalysator hangt af van de specifieke reactie die u probeert uit te voeren.
Belangrijkste verschillen:
* Zuurgraad: Natriumacetaat is een zwakke base, terwijl zwavelzuur een sterk zuur is.
* Reactietypen: Natriumacetaat wordt vaak gebruikt bij door base gekatalyseerde reacties, terwijl zwavelzuur vaak wordt gebruikt bij door zuur gekatalyseerde reacties.
* Voorwaarden: De reactieomstandigheden (temperatuur, concentratie, enz.) zullen ook een rol spelen bij het kiezen van de geschikte katalysator.
Samenvattend is er geen "betere" katalysator; elk is beter geschikt voor verschillende reacties op basis van hun specifieke eigenschappen.
 Nieuwe generatie kooldioxidegasscheidingssysteem met adsorbentia van het gate-type
Nieuwe generatie kooldioxidegasscheidingssysteem met adsorbentia van het gate-type Wat is substraatconcentratie?
Wat is substraatconcentratie?  Microanalyse van biologische monsters voor vroege detectie van ziekten
Microanalyse van biologische monsters voor vroege detectie van ziekten Welke eigenschappen zijn gebruikelijk voor zowel zuren als basen?
Welke eigenschappen zijn gebruikelijk voor zowel zuren als basen?  Wat gebeurt er met een stof als deze wordt gekoeld?
Wat gebeurt er met een stof als deze wordt gekoeld?
Hoofdlijnen
- Welke theorie verklaarde dat organismen zijn geëvolueerd van een gemeenschappelijke voorouder?
- Wat is het doel van ribosomen?
- De 20 aminozuren:een uitgebreide lijst en gids
- Wat is de naam van structuur waarin een bevrucht ei groeit en zich ontwikkelt tot baby?
- Subeenheden van de Amerikaanse overheid worden genoemd?
- Waar kan ik een Glencoe -biologieboek vinden bij online?
- Braziliaanse onderzoekers ontdekken zes nieuwe soorten zijdemiereneter
- Welke organismen zijn prokaryotisch-?
- Is er DNA in planten- of dierlijke cellen?
- Amorfe diamant gesynthetiseerd

- Nieuwe modellen om de microstructuur van polymeermengsels te onderzoeken

- Verbetering van condensatie:op weg naar praktische energie- en watertoepassingen

- Schimmel Rode Zee levert aanknopingspunten voor nieuwe medicijnen tegen epilepsie
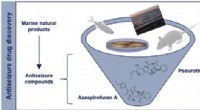
- De grenzen van een nieuw soort chemo verkennen
 Welk type binding is waarschijnlijk betrokken bij de monsters die in hun pure vorm geen geleiders waren, maar een stroom geleidden wanneer ze zich vermengden met water?
Welk type binding is waarschijnlijk betrokken bij de monsters die in hun pure vorm geen geleiders waren, maar een stroom geleidden wanneer ze zich vermengden met water?  Waarom gebeurt het verwarmingseffect van elektrische stroom?
Waarom gebeurt het verwarmingseffect van elektrische stroom?  Wat is het plantenleven dat op natuurlijke wijze groeit op een plek?
Wat is het plantenleven dat op natuurlijke wijze groeit op een plek?  Als K en L -shell van een atoom vol zijn, wat zijn dan de nummerelektronen in Atom?
Als K en L -shell van een atoom vol zijn, wat zijn dan de nummerelektronen in Atom?  Hoe is het oppervlak van de aarde?
Hoe is het oppervlak van de aarde?  Hoe zijn basic chemische elementen betrokken bij de vorming van biomoleculen?
Hoe zijn basic chemische elementen betrokken bij de vorming van biomoleculen?  Wat is de menselijke relevantie van gymnospermen?
Wat is de menselijke relevantie van gymnospermen?  Fotopyro-elektrische microfluïdica ontwikkeld door onderzoekers
Fotopyro-elektrische microfluïdica ontwikkeld door onderzoekers
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

