
Wetenschap
Lithiumreactiviteit:reacties met zuren en basen uitgelegd
Reactie met zuren:
* Mechanisme: Lithium is een zeer reactief alkalimetaal. Wanneer het in contact komt met een zuur, staat het gemakkelijk een elektron af aan de waterstofionen (H+) die in het zuur aanwezig zijn. Dit resulteert in de vorming van lithiumionen (Li+) en waterstofgas (H2).
* Voorbeeld:
* 2Li(s) + 2HCl(aq) → 2LiCl(aq) + H2(g)
* Reactiekenmerken: Deze reacties zijn exotherm, waarbij warmte vrijkomt en een krachtige ontwikkeling van waterstofgas ontstaat.
Reactie met basen:
* Mechanisme: Hoewel lithium niet zo reactief is met basen als met zuren, kan het nog steeds reageren. In dit geval reageert lithium met de hydroxide-ionen (OH-) die in de base aanwezig zijn, waarbij lithiumhydroxide (LiOH) en waterstofgas worden gevormd.
* Voorbeeld:
* 2Li(s) + 2H2O(l) → 2LiOH(aq) + H2(g)
* Reactiekenmerken: De reactie is minder krachtig dan bij zuren, maar er komt nog steeds warmte vrij en er ontstaat waterstofgas.
Belangrijke opmerkingen:
* Veiligheid: Reacties van lithium met zuren en basen zijn zeer exotherm en kunnen gevaarlijk zijn. Ga altijd voorzichtig om met lithium en in een goed geventileerde ruimte.
* Reactiepercentage: De reactiviteit van lithium met zuren en basen wordt beïnvloed door de concentratie van het zuur of de base, de temperatuur en het oppervlak van het lithium.
Laat het me weten als je nog vragen hebt!
 Als ademhaling koolstofdioxide en water produceert, wat gebeurt er dan met deze producten voor dat ze in het lichaam worden opgebouwd?
Als ademhaling koolstofdioxide en water produceert, wat gebeurt er dan met deze producten voor dat ze in het lichaam worden opgebouwd?  Waarom zuurstof een mineraal?
Waarom zuurstof een mineraal?  Een op ruthenium gebaseerde katalysator met zeer actieve, vlakke oppervlakken presteren beter dan op metaal gebaseerde concurrenten
Een op ruthenium gebaseerde katalysator met zeer actieve, vlakke oppervlakken presteren beter dan op metaal gebaseerde concurrenten Oplossing voor raadselachtig fenomeen kan de deur openen naar verbeterde koude sproei-efficiëntie
Oplossing voor raadselachtig fenomeen kan de deur openen naar verbeterde koude sproei-efficiëntie Nieuwe katalysator verbetert broeikasgas tot hernieuwbare koolwaterstoffen
Nieuwe katalysator verbetert broeikasgas tot hernieuwbare koolwaterstoffen
Hoofdlijnen
- Welk orgaan bestaat uit zowel endocrien als exocrien weefsel?
- Welk type cellen worden geproduceerd na bemesting en de gameten combineren?
- Wat is het Genotype voor de Roan-kleur?
- Wat is de wetenschappelijke naam voor muggen?
- Leg uit waarom levende wezens die in hetzelfde geslacht zijn geclassificeerd, meer op elkaar lijken dan die klasse?
- Wat is het kenmerk van organismen die behoren tot Kingdom Monera?
- Waarom gapen besmettelijk is bij bonobo's
- Welke lichaamssystemen gebruiken antilichamen eiwitten en gespecialiseerde cellen om de van infectieziekten te verdedigen?
- Welke organel omringt elke cel?
- Nieuw NIST-onderzoek kan de kosten van het maken van stuivers verlagen

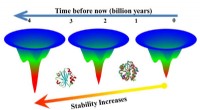
- Eiwitten die tegen de hitte kunnen
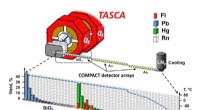
- Onderzoek toont aan dat flerovium het meest vluchtige metaal is in het periodiek systeem
- Zelfassemblerende materialen kunnen patronen vormen die nuttig kunnen zijn in optische apparaten

- Slimmer verwarmen, niet moeilijker:hoe microgolven katalytische reacties efficiënter maken

 De 210 miljoen jaar oude Smok verpletterde botten als een hyena
De 210 miljoen jaar oude Smok verpletterde botten als een hyena Hoe kan halfgeleidermateriaal worden gemaakt om een geleider of een isolator te worden?
Hoe kan halfgeleidermateriaal worden gemaakt om een geleider of een isolator te worden?  Luchtvervuiling daalde, plasticgebruik steeg enorm tijdens Europa-lockdowns
Luchtvervuiling daalde, plasticgebruik steeg enorm tijdens Europa-lockdowns Meer wetenschappelijke expertise nodig in Parlement om besluitvorming te verbeteren
Meer wetenschappelijke expertise nodig in Parlement om besluitvorming te verbeteren Oude metalen ketels geven ons aanwijzingen over wat mensen in de bronstijd aten
Oude metalen ketels geven ons aanwijzingen over wat mensen in de bronstijd aten  Salesforce koopt Tableau Software in een deal van $ 15,7 miljard in aandelen
Salesforce koopt Tableau Software in een deal van $ 15,7 miljard in aandelen Wat omvat een ecosysteem?
Wat omvat een ecosysteem?  Wat kan goed werken zonder energie te verspillen?
Wat kan goed werken zonder energie te verspillen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

