
Wetenschap
Elektronenconfiguratie en de Octetregel:Magnesium als voorbeeld
Magnesium's elektronenconfiguratie:
* Magnesium heeft een atoomnummer van 12, wat betekent dat het 12 protonen en 12 elektronen heeft.
* De elektronenconfiguratie is 1s² 2s² 2p⁶ 3s².
* Dit betekent dat het buitenste energieniveau (het 3e energieniveau) slechts 2 elektronen in de 3s-orbitaal heeft.
De Octetregel:
* De octetregel stelt dat atomen de neiging hebben om elektronen te winnen, te verliezen of te delen om een stabiele configuratie te bereiken met 8 elektronen in hun buitenste energieniveau (valentieschil).
* Deze stabiele configuratie is vergelijkbaar met de edelgassen, die zeer niet-reactief zijn.
Magnesiumoplossing:
* Magnesium heeft slechts 2 valentie-elektronen, dus het moet er nog 6 winnen om een octet te bereiken.
* Magnesium kan echter gemakkelijker verliezen zijn 2 valentie-elektronen om de stabiele configuratie van het vorige edelgas te bereiken (neon, met 10 elektronen, 2 in de eerste schil en 8 in de tweede).
*Door het verlies van deze elektronen wordt magnesium een positief geladen ion (Mg²⁺) met een volledige buitenschil van 8 elektronen ten opzichte van het vorige energieniveau.
Vorming van een ionische binding:
* Magnesium kan dan een ionische binding vormen met een element zoals chloor (Cl), dat 7 valentie-elektronen heeft.
* Chloor heeft 1 elektron nodig om zijn octet te voltooien en wordt een negatief geladen ion (Cl⁻).
* De elektrostatische aantrekkingskracht tussen het positief geladen magnesiumion (Mg²⁺) en het negatief geladen chloorion (Cl⁻) vormt een ionische binding, resulterend in de verbinding magnesiumchloride (MgCl₂).
Samenvattend bereikt magnesium een volledige buitenste schil door zijn twee valentie-elektronen te verliezen en een positief geladen ion te worden. Hierdoor kan het een ionische binding vormen met andere atomen om stabiliteit te bereiken.
 Woordvergelijking voor lithiumoxide en water?
Woordvergelijking voor lithiumoxide en water?  Waarom stopte het mengsel met het blauw kleuren van druppels jodiumoplossing na 240 seconden?
Waarom stopte het mengsel met het blauw kleuren van druppels jodiumoplossing na 240 seconden?  Studie van olifant, capibara, mensenhaar vindt dat dikker haar niet altijd sterker is
Studie van olifant, capibara, mensenhaar vindt dat dikker haar niet altijd sterker is Zelfherstellende katalysatorfilms voor waterstofproductie
Zelfherstellende katalysatorfilms voor waterstofproductie Wat is de Comtributon van Robert Boyle in de Atomic -theorie van de ontwikkeling?
Wat is de Comtributon van Robert Boyle in de Atomic -theorie van de ontwikkeling?
Hoofdlijnen
- Ziekteverwekkers identificeren die sojastamkanker veroorzaken
- Is het levend of dood? Team laat zien hoe je de thermische handtekeningen van afzonderlijke cellen kunt meten
- Waarom deden wetenschappers zo lang om te concluderen dat alle levende dingen van cellen zijn gemaakt, zelfs met de hulp van een microscoop?
- Wat is het doel van cytoplasma?
- Welke nucleotiden worden gebruikt om RNA te bouwen?
- Heeft het virus gespecialiseerde structuren of interne compartimenten?
- Eiwitten bestemd voor export vanuit de cel worden gesynthetiseerd met een signaalsequentie en beginnen hun synthese?
- Welke drie kritische genfuncties identificeerden wetenschappers?
- Welke vorm van natuurlijke selectie speelt het meest waarschijnlijk een rol bij speciatie?
- Ingebed gasdetectieapparaat belooft eenvoudig, nauwkeurige detectie van vluchtige organische stoffen

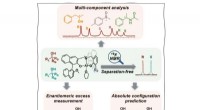
- Fluor maakt scheidingsvrije chirale chromatografische analyse mogelijk
- Nieuwe theorie over kruisverschijnselen kan de effectiviteit van nieuwe materialen voorspellen

- Onderzoeksteam streeft ernaar de kosten van medicijnontwikkeling te verlagen met behulp van 3D-geprinte levende weefsels

- Waarom het periodiek systeem is gestructureerd op basis van atoomnummer:rijen en kolommen uitgelegd

 Wie heeft thermische energie -energie uitgevonden?
Wie heeft thermische energie -energie uitgevonden?  Waarom worden resterende bergen ook genoemd naar denudatie?
Waarom worden resterende bergen ook genoemd naar denudatie?  Nieuwe tool geeft appelboerderijen hoop in strijd tegen voorjaarsbevriezing
Nieuwe tool geeft appelboerderijen hoop in strijd tegen voorjaarsbevriezing Welke planeet in uw zonnestelsel heeft de snelste rotatiesnelheid?
Welke planeet in uw zonnestelsel heeft de snelste rotatiesnelheid?  Wat zijn drie oorzaken van erosie?
Wat zijn drie oorzaken van erosie?  Hoe de aarde te vergelijken met Neptunus
Hoe de aarde te vergelijken met Neptunus  Hooggerechtshof in Europa zal baanbrekende klimaatvonnissen uitvaardigen
Hooggerechtshof in Europa zal baanbrekende klimaatvonnissen uitvaardigen  De laagste hoogte -beperkende stroom erosie wordt genoemd?
De laagste hoogte -beperkende stroom erosie wordt genoemd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

