
Wetenschap
Ideale gaswet:gasgedrag en -formule begrijpen
* Druk (P): De kracht die door de gasmoleculen op de wanden van hun container wordt uitgeoefend.
* Volume (V): De ruimte die door het gas wordt ingenomen.
* Temperatuur (T): Een maat voor de gemiddelde kinetische energie van de gasmoleculen.
* Hoeveelheid gas (n): Meestal gemeten in mol.
De ideale gaswet wordt weergegeven door de volgende vergelijking:
PV =nRT
Waar:
* R is de ideale gasconstante, een waarde die rekening houdt met de relatie tussen de andere variabelen.
Belangrijke aannames van de ideale gaswet:
* Gasmoleculen hebben geen volume: Dit betekent dat de moleculen worden beschouwd als puntmassa's met een verwaarloosbare grootte in vergelijking met de ruimte die ze innemen.
* Gasmoleculen hebben geen interactie met elkaar: Dit impliceert dat er tussen hen geen aantrekkende of afstotende krachten bestaan.
* Botsingen tussen gasmoleculen en de containerwanden zijn perfect elastisch: Dit betekent dat er bij botsingen geen kinetische energie verloren gaat.
Ideaal gedrag versus echt gedrag:
Hoewel de ideale gaswet een nuttig raamwerk biedt voor het begrijpen van gasgedrag, wijken echte gassen onder bepaalde omstandigheden af van ideaal gedrag, zoals:
* Hoge druk: Bij hoge drukken bevinden de gasmoleculen zich dichter bij elkaar en wordt hun volume aanzienlijk vergeleken met de ruimte die ze innemen.
* Lage temperatuur: Bij lage temperaturen worden de aantrekkingskrachten tussen gasmoleculen groter, wat leidt tot afwijkingen van het ideale gedrag.
Ondanks deze afwijkingen blijft de ideale gaswet een krachtig hulpmiddel voor het voorspellen en verklaren van het gedrag van gassen onder veel omstandigheden.
 Poreus kristal leidt reactie om koolstofdioxide te transformeren
Poreus kristal leidt reactie om koolstofdioxide te transformeren Waar worden zwavelpillen voor gebruikt?
Waar worden zwavelpillen voor gebruikt?  Oxidatietoestanden van reacties tussen kaliumoxide en koolstofdioxide?
Oxidatietoestanden van reacties tussen kaliumoxide en koolstofdioxide?  Hoe de molariteit van een oplossing te veranderen
Hoe de molariteit van een oplossing te veranderen  Wat is de molecuulformule van een verbinding met een empirische C4H9 en een grammassa van 114 gram mol?
Wat is de molecuulformule van een verbinding met een empirische C4H9 en een grammassa van 114 gram mol?
 Welke wetenschap werd beïnvloed door de wetenschappelijke revolutie?
Welke wetenschap werd beïnvloed door de wetenschappelijke revolutie?  Vulkaan op Indonesië Java gutst as, veroorzaakt paniek
Vulkaan op Indonesië Java gutst as, veroorzaakt paniek Wetenschappers gebruiken oude zeefossielen om al lang bestaande klimaatpuzzel te ontrafelen
Wetenschappers gebruiken oude zeefossielen om al lang bestaande klimaatpuzzel te ontrafelen Recente opwarming van de Atlantische Oceaan ongekend in bijna 3, 000 jaar
Recente opwarming van de Atlantische Oceaan ongekend in bijna 3, 000 jaar Bliksem doodt 22 doden in Bangladesh
Bliksem doodt 22 doden in Bangladesh
Hoofdlijnen
- Stadia van ecologische successie
- Uit een tuinonderzoek van Three Sisters blijkt dat een evenwichtig netwerk van bestuivers en planten een onzekere toekomst tegemoet gaat
- Welke twee factoren kunnen denatureren van een enzym veroorzaken?
- Hoe je winnaar kunt worden in het evolutiespel
- Welk element wordt gevonden in eiwitten en DNA?
- Welk huishoudelijke Procict bevat enzymen?
- Wat is een organisme dat de hele of een andere roept doodt en eet?
- Soorten berekenen Evenness
- Nieuwe plantibodies zijn veelbelovend om citrus te beschermen tegen vergroeningsziekten
- Hoogwaardige elektrokatalysatoren om de ontwikkeling van directe ethanolbrandstofcellen te stimuleren

- In woestijnproeven, wateroogstmachine van de volgende generatie levert vers water uit de lucht
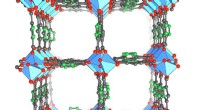
- Drie begeleiders coördineren het uiteenvallen van amyloïde fibrillen in gist
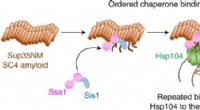
- Onder druk:eiwit-nabootsende moleculen manipuleren met hydrostatische druk
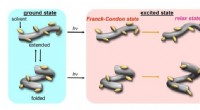
- Polyethyleen:de basis van moderne kunststoffen

 Bereken de molariteit:voorbereiding van de oplossing en stoichiometrie - voorbeeld
Bereken de molariteit:voorbereiding van de oplossing en stoichiometrie - voorbeeld  Voorbeelden waarbij de snelheid nul is, maar geen versnelling?
Voorbeelden waarbij de snelheid nul is, maar geen versnelling?  Is de gum een geleider of isolator?
Is de gum een geleider of isolator?  Nieuwe studie onthult geheimen van evolutie op moleculair niveau
Nieuwe studie onthult geheimen van evolutie op moleculair niveau NASA ziet tropische depressie Rene verdwijnen
NASA ziet tropische depressie Rene verdwijnen Branding van energiebedrijven, geen deals, beïnvloedt het wisselen van klant
Branding van energiebedrijven, geen deals, beïnvloedt het wisselen van klant Kilonovae:De standaardkaars in zijn eigen nest in een hinderlaag lokken
Kilonovae:De standaardkaars in zijn eigen nest in een hinderlaag lokken Zwavelzuur- en natriumhydroxidereactie:chemische vergelijking en uitleg
Zwavelzuur- en natriumhydroxidereactie:chemische vergelijking en uitleg
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

