
Wetenschap
Moleculaire samengestelde formules:moeten ladingen in evenwicht worden gebracht?
* Moleculaire verbindingen worden gevormd door niet-metalen. Niet-metalen delen elektronen om covalente bindingen te vormen, wat betekent dat ze geen elektronen winnen of verliezen om ionen met positieve of negatieve ladingen te vormen.
* Er zijn geen ionen aanwezig. Omdat er geen ionen zijn, zijn er geen kosten die in evenwicht moeten worden gebracht.
* De formule weerspiegelt de verhouding van atomen. De subscripts in de formule geven eenvoudigweg de verhouding van elk element in het molecuul aan.
Voorbeeld:
* Water (H₂O) heeft twee waterstofatomen en één zuurstofatoom. De formule houdt geen rekening met het balanceren van ladingen, omdat de waterstof- en zuurstofatomen elektronen delen om covalente bindingen te vormen.
In tegenstelling daarmee:
* Ionische verbindingen worden gevormd door metalen en niet-metalen, die ionen vormen met positieve en negatieve ladingen. Deze ladingen moeten *wel* in evenwicht worden gebracht om een neutrale verbinding te creëren.
Voorbeeld:
* Natriumchloride (NaCl) heeft één natriumion (Na⁺) en één chloride-ion (Cl⁻). De formule weerspiegelt de balans tussen de +1 lading natrium en de -1 lading chloride.
 Mechanisme van splitsing van waterstofbruggen op ijzerbasis onthuld
Mechanisme van splitsing van waterstofbruggen op ijzerbasis onthuld Inzicht in 9-koolstofkoolhydraten:formules en structuren
Inzicht in 9-koolstofkoolhydraten:formules en structuren  Onderzoekers observeren de reactie van silicaatglas met waterige oplossingen in realtime
Onderzoekers observeren de reactie van silicaatglas met waterige oplossingen in realtime Wat betekent een gevaarlijk chemisch teken?
Wat betekent een gevaarlijk chemisch teken?  Welk type binding heeft het grootste verschil in elektronegativiteit?
Welk type binding heeft het grootste verschil in elektronegativiteit?
 Waarom vallen vogels niet om als ze springen?
Waarom vallen vogels niet om als ze springen?  Wil je dat burgers zich zorgen maken over klimaatverandering? Schrijf ze een cheque
Wil je dat burgers zich zorgen maken over klimaatverandering? Schrijf ze een cheque Wat betekent de naam Amber anders dan gefossiliseerde boomsap?
Wat betekent de naam Amber anders dan gefossiliseerde boomsap?  Rijke landen komen te kort bij toezegging klimaatfinanciering
Rijke landen komen te kort bij toezegging klimaatfinanciering Bosbranden leiden tot evacuaties in Noord-Californië
Bosbranden leiden tot evacuaties in Noord-Californië
Hoofdlijnen
- Wat zijn niet -voorbeelden van prokaryote?
- Wat zijn de twee organismen die zuurstof bieden voor sfeer?
- Fossielen onthullen hoe bizarre zoogdieren het uitsterven verslaan
- Onderzoek beschrijft hoe sommige vissen omgaan met parasieten, wat gevolgen heeft voor de menselijke gezondheid
- De zes essentiële elementen van het leven:koolstof, waterstof, zuurstof, stikstof, fosfor en zwavel
- Drie ding maken de structuur van een DNA -molecuul?
- Wat is de wetenschappelijke term voor een ei?
- Wat is een voorbeeld van Epiphora?
- Welke informatie bepaalt allelen?
- Natriumbicarbonaat:fysische en chemische eigenschappen uitgelegd

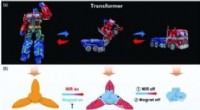
- Magnetisch gestuurd, op hydrogel gebaseerde slimme transformatoren
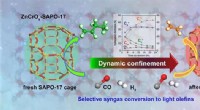
- Dynamische opsluiting van SAPO-17-kooien op selectiviteitscontrole van syngasconversie
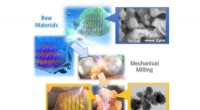
- Nieuw elektrodemateriaal ontwikkeld om de laadcapaciteit van lithiumbatterijen te vergroten
- Hoe chemicaliën olie afbreken:dispergeermiddelen, bioremediatie, zonlicht en het opruimen van dieren

 Waarom worden protozoanen vaak aangezien voor rotifers?
Waarom worden protozoanen vaak aangezien voor rotifers?  Waarom zijn oudere sterren in het midden van een spiraalvormige sterrenstelsel terwijl jongere make -up wapens in de make -up?
Waarom zijn oudere sterren in het midden van een spiraalvormige sterrenstelsel terwijl jongere make -up wapens in de make -up?  Welk orgaan is nodig in een aseksuele reproductie?
Welk orgaan is nodig in een aseksuele reproductie?  Archeoloog onthult verborgen geschiedenis van conquistadores in het Zuiden van Amerika
Archeoloog onthult verborgen geschiedenis van conquistadores in het Zuiden van Amerika Welke rol speelt afval in aquatische ecosystemen?
Welke rol speelt afval in aquatische ecosystemen?  Hoe beïnvloedt snelheid het momentum?
Hoe beïnvloedt snelheid het momentum?  Zijn sedimentaire rotsen gemaakt van stukken andere rotsen?
Zijn sedimentaire rotsen gemaakt van stukken andere rotsen?  Onderzoekers voeren chemische studie uit van een oude, metaalrijke bolvormige sterrenhoop
Onderzoekers voeren chemische studie uit van een oude, metaalrijke bolvormige sterrenhoop
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

