
Wetenschap
Berekening van de pH van HCl- en NaOH-mengsels:een stapsgewijze handleiding
* Neutralisatiereactie: HCl (een sterk zuur) en NaOH (een sterke base) reageren in een molaire verhouding van 1:1 en vormen water (H2O) en zout (NaCl):
HCl + NaOH → H2O + NaCl
* Molariteit en volume: De pH van de uiteindelijke oplossing hangt af van de hoeveelheid overtollig zuur of base die overblijft na de reactie. Dit wordt bepaald door de initiële volumes van de HCl- en NaOH-oplossingen.
Voorbeeldscenario's:
* Gelijke volumes: Als je gelijke volumes 1N HCl en 1N NaOH mengt, wordt de oplossing perfect geneutraliseerd, wat resulteert in een pH van 7 (neutraal).
* Meer HCl: Als u meer HCl dan NaOH heeft, zal de resulterende oplossing zuur zijn en zal de pH lager zijn dan 7.
* Meer NaOH: Als u meer NaOH dan HCl heeft, zal de resulterende oplossing basisch zijn en zal de pH groter zijn dan 7.
De pH berekenen:
1. Bepaal het aantal mol HCl en NaOH:
* mol =Molariteit (N) x Volume (L)
2. Identificeer de beperkende reactant: De reactant met minder mol is de beperkende reactant.
3. Bereken het aantal mol overtollige reactant: Trek het aantal mol beperkende reactant af van het aantal mol overtollige reactant.
4. Bereken de concentratie van de overtollige reactant: Deel het aantal mol overtollige reactant door het totale volume van het mengsel.
5. Bepaal de pH:
* Als de overtollige reactant HCl is:pH =-log[H+]
* Als de overtollige reactant NaOH is:pOH =-log[OH-], dan pH =14 - pOH
Onthoud: Werk altijd met volumes in liters (L) voor nauwkeurige berekeningen.
 Wanneer koolstof reageert met een zuur, welk gas wordt er uitgegeven?
Wanneer koolstof reageert met een zuur, welk gas wordt er uitgegeven?  Nabij-infrarood reflecterende mengcoatings hebben betere optische en koelprestaties
Nabij-infrarood reflecterende mengcoatings hebben betere optische en koelprestaties Zuur-basereacties:zout- en watervorming begrijpen
Zuur-basereacties:zout- en watervorming begrijpen  Hoe wordt het genoemd als luchtmoleculen bij elkaar worden verpakt?
Hoe wordt het genoemd als luchtmoleculen bij elkaar worden verpakt?  Hoe de oxidatietoestand van CH4 op te lossen
Hoe de oxidatietoestand van CH4 op te lossen
 Waar gaan alle muggen heen in de winter?
Waar gaan alle muggen heen in de winter?  Stalagmieten in droge corridor suggereren dat Amazonia bossen heeft onderhouden tijdens de laatste ijstijd
Stalagmieten in droge corridor suggereren dat Amazonia bossen heeft onderhouden tijdens de laatste ijstijd Waar is 's werelds grootste Bald Eagle-bevolking?
Waar is 's werelds grootste Bald Eagle-bevolking?  Beschouwingen over COVID-19 en onze vernietiging van de natuur
Beschouwingen over COVID-19 en onze vernietiging van de natuur Wat is het verschil tussen wetenschappelijke methode en houding?
Wat is het verschil tussen wetenschappelijke methode en houding?
Hoofdlijnen
- Welke structuren worden in alle cellen gevonden?
- Onderzoek werpt licht op hoe bladsnijdermieren chemische afscheidingen gebruiken om schimmelinfecties te voorkomen
- Wat is een enylena alsjeblieft, ik heb een antwoord nodig voor mijn examen op cellen?
- Welke celverbinding mogelijk maakt de beweging van moleculen tussen twee plantencellen mogelijk?
- Wat voor soort organisme bestaat uit prokaryotische cellen?
- De celorganellen die helpen bij divisie zijn de?
- Welk einde definieert enzymnamen? Het achtervoegsel '-ase' begrijpen
- Welke rol speelt mitochondria?
- Welk type transport vereist ATP om moleculen te verplaatsen?
- Onderzoekers kijken naar interactie tussen olie en water om waterverontreiniging te voorkomen

- Een celdeurbel begrijpen
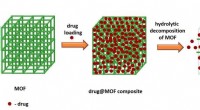
- Voeg gewoon water toe:scheikundigen suggereren een oplossing voor onoplosbare medicijnen
- Mager elektrolytontwerp is een game-changer voor magnesiumbatterijen

- Minimalisering van blootstelling aan schadelijke vlamvertragende chemicaliën in afvalschuim en kunststoffen

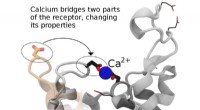
 Een ionische verbinding van calcium en chloor zou worden genoemd?
Een ionische verbinding van calcium en chloor zou worden genoemd?  Waar is de potentiële energie van doos het grootst op helling?
Waar is de potentiële energie van doos het grootst op helling?  Waarom verhuizen zoveel vluchtelingen na aankomst? Kans en gemeenschap
Waarom verhuizen zoveel vluchtelingen na aankomst? Kans en gemeenschap Komt u zonder fossiele brandstoffen of kernenergie meer?
Komt u zonder fossiele brandstoffen of kernenergie meer?  Het verborgen gevaar:sneeuw scheppen kan fatale hartaanvallen veroorzaken
Het verborgen gevaar:sneeuw scheppen kan fatale hartaanvallen veroorzaken  Waarom drijft de ene substantie over de andere?
Waarom drijft de ene substantie over de andere?  Hoewel metalen en zouten vergelijkbare roosterstructuren hebben, zijn goede materialen voor elektrische bedrading, waarom in plaats daarvan?
Hoewel metalen en zouten vergelijkbare roosterstructuren hebben, zijn goede materialen voor elektrische bedrading, waarom in plaats daarvan?  Wat is Beryllium massa -nummer?
Wat is Beryllium massa -nummer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

