
Wetenschap
Het vriesproces:de overgang van vloeistof naar vaste stof begrijpen
* Verlaagde kinetische energie: De moleculen in een vloeistof zijn voortdurend in beweging en botsen met elkaar. Wanneer de vloeistof wordt afgekoeld, daalt de temperatuur, wat betekent dat de moleculen minder kinetische energie hebben. Hierdoor vertragen ze.
* Verkleinde afstand: Naarmate de moleculen vertragen, verliezen ze het vermogen om de aantrekkingskracht tussen hen te overwinnen. Dit zorgt ervoor dat de moleculen dichter bij elkaar komen, waardoor de afstand ertussen kleiner wordt.
* Vorming van een regelmatig rooster: Met de kleinere afstand en langzamere beweging worden de moleculen beter georganiseerd en rangschikken ze zichzelf in een vast, zich herhalend patroon dat een kristalrooster wordt genoemd. Dit geeft de vaste stof zijn stijve structuur.
* Statuswijziging: Zodra de moleculen in het kristalrooster zijn opgesloten, is de substantie overgegaan van een vloeistof naar een vaste stof. Deze kenmerkt zich door een vast volume en vorm.
Belangrijke dingen om te onthouden over bevriezen:
* Temperatuur blijft constant: Tijdens het bevriezen blijft de temperatuur van de substantie constant, ook al wordt warmte verwijderd. Dit komt omdat de warmte-energie wordt gebruikt om de bindingen tussen moleculen in vloeibare toestand te verbreken.
* Vriespunt: Elke stof heeft een specifiek vriespunt waarop deze overgaat van vloeibaar naar vast. Dit punt wordt bepaald door de sterkte van de intermoleculaire krachten tussen de moleculen.
Voorbeelden van bevriezing:
* Water bevriest tot ijs
* Gesmolten lava stolt tot gesteente
* Vloeibaar kwik verandert in vast kwik
Laat het me weten als je dieper wilt ingaan op de wetenschap achter bevriezing, of als je specifieke vragen hebt!
 NASA ziet tropische cycloon 16P zich ontwikkelen
NASA ziet tropische cycloon 16P zich ontwikkelen Tweets blijken een betrouwbare indicator te zijn voor de luchtkwaliteit tijdens bosbranden
Tweets blijken een betrouwbare indicator te zijn voor de luchtkwaliteit tijdens bosbranden Hoe noemt het bos niet dat je een jungle schuilt?
Hoe noemt het bos niet dat je een jungle schuilt?  Een al lang bestaand mysterie oplossen over het canvas van de woestijnrotskunst
Een al lang bestaand mysterie oplossen over het canvas van de woestijnrotskunst Klimaatverandering:drie manieren om de wetenschap op de markt te brengen om de sceptici te bereiken
Klimaatverandering:drie manieren om de wetenschap op de markt te brengen om de sceptici te bereiken
Hoofdlijnen
- Wat is een biologische metafoor?
- Wat is in een eukaryote een segment van gen dat codeert voor eiwitten?
- Een elektrolytendrank met kipsmaak kan snuffelhonden helpen gehydrateerd te blijven
- Wat voor soort bacteriën zou waarschijnlijk een ziekte veroorzaken?
- De weggelopen paarden in Londen herinneren ons eraan dat dieren ook werkers zijn
- Wat is het gebruik en de toepassing van de biologische wetenschap?
- Wat is het bloemblad van de plant?
- Wat is een subarachnoïdale bloeding?
- Hoe elimineer je een virus in planten?
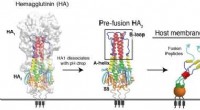
- Onderzoekers vinden nieuwe manier om griepvirus aan te pakken
- Interfacing met de hersenen
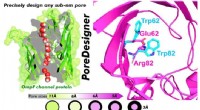
- PoreDesigner verbetert het ontwerp van eiwitkanalen voor waterbehandeling, bioscheidingen
- Mechanisme van splitsing van waterstofbruggen op ijzerbasis onthuld

- Nieuwe fotonische vloeibare kristallen kunnen leiden tot displays van de volgende generatie

 Wat zijn de meest voorkomende opdringerige en extrusieve rotsen?
Wat zijn de meest voorkomende opdringerige en extrusieve rotsen?  Welke organel wordt geassocieerd met een syntheseproces?
Welke organel wordt geassocieerd met een syntheseproces?  Onderzoek onderzoekt hoe nadenken over je waarden voordat je je mond opendoet, zorgt voor gelukkiger relaties
Onderzoek onderzoekt hoe nadenken over je waarden voordat je je mond opendoet, zorgt voor gelukkiger relaties  Wat zaagvissen werkelijk doen met hun zaag
Wat zaagvissen werkelijk doen met hun zaag  Waar zou je de grond vinden die Silty Soil wordt genoemd?
Waar zou je de grond vinden die Silty Soil wordt genoemd?  Temperatuurschaalconversie Een stuk droogijs vaste CO2 heeft temperatuur -100c Wat is het in Kelvins en graden F?
Temperatuurschaalconversie Een stuk droogijs vaste CO2 heeft temperatuur -100c Wat is het in Kelvins en graden F?  GM's nieuwste voertuig:off-road, zelfrijdende rover voor de maan
GM's nieuwste voertuig:off-road, zelfrijdende rover voor de maan 100 miljoen dode bomen in de Sierra vormen een enorm risico voor onvoorspelbare bosbranden
100 miljoen dode bomen in de Sierra vormen een enorm risico voor onvoorspelbare bosbranden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

