
Wetenschap
Zuurgraad van functionele groepen:hoe functionele groepen de pH in biologische moleculen beïnvloeden
Door Matthew Williams
Bijgewerkt op 30 augustus 2022
mmoxley/iStock/GettyImages
Al het leven op aarde is opgebouwd uit vier fundamentele klassen van organische moleculen:koolhydraten, lipiden, eiwitten en nucleïnezuren. Elk bevat koolstof en waterstof, en hun eigenschappen worden bepaald door de functionele groepen die aan het koolstofskelet zijn bevestigd. Terwijl veel functionele groepen de zuurgraad van een molecuul onveranderd laten, kunnen andere de pH van de biologische vloeistoffen waarin ze zich bevinden dramatisch veranderen. Het begrijpen van deze interacties is cruciaal voor het behouden van het fysiologische evenwicht.
Zuren, basen en de pH-schaal
De pH-schaal (0–14) kwantificeert de concentratie waterstofionen (H⁺) ten opzichte van hydroxide-ionen (OH⁻). Bij pH 7 zijn de getallen H⁺ en OH⁻ gelijk, wat neutraliteit vertegenwoordigt. Stoffen die de H⁺-concentratie verhogen verlagen de pH (zuur, 0–6,9), terwijl stoffen die OH⁻ verhogen of H⁺ binden de pH verhogen (basisch, 7,1–14). Hoe verder de pH van een oplossing afwijkt van 7, hoe groter de potentiële biologische impact. Maagzuur heeft bijvoorbeeld een pH 2, terwijl industriële loog de pH 13 kan overschrijden.
Functionele groepen die de zuurgraad niet significant beïnvloeden
De meeste functionele groepen, zoals ketonen, eenvoudige hydroxylen, aldehyden en sulfhydrylen, doneren of accepteren over het algemeen geen protonen onder fysiologische omstandigheden, zodat ze een minimale invloed uitoefenen op de algehele pH van een molecuul. Hun elektronische structuren en bindingspatronen houden ze grotendeels neutraal in waterige omgevingen.
Carboxylgroepen (–COOH)
Carboxylgroepen zijn klassieke zure functionele groepen. De hoge elektronegativiteit van zuurstofatomen stabiliseert de negatieve lading die ontstaat wanneer de hydroxylwaterstof vrijkomt als H⁺. Deze protonenafgifte verlaagt de pH van de omringende oplossing. Carboxylgroepen zijn aanwezig in vetzuren, fosfolipiden en aminozuren, waardoor ze centraal staan in veel biochemische processen.
Fosfaatgroepen (–PO₄³⁻)
Fosfaatgroepen kunnen tot twee protonen per molecuul doneren, waardoor ze sterk zuur worden. Met vier zuurstofatomen die fosfor omringen, kan het molecuul na deprotonering de negatieve lading stabiliseren, waardoor protonen gemakkelijk kunnen dissociëren. Fosfaten zijn sleutelcomponenten van nucleïnezuren, ATP en veel signaalmoleculen.
Aminogroepen (–NH₂)
Aminogroepen fungeren als basen:het eenzame paar op stikstof kan een proton accepteren, waardoor de lokale pH stijgt. Bij aminozuren werken de carboxyl- en aminogroepen doorgaans samen:carboxylgroepen doneren H⁺ terwijl aminogroepen H⁺ accepteren, wat vaak resulteert in een neutraal netto-effect op de pH onder fysiologische omstandigheden.
Door de zure of basische aard van functionele groepen te begrijpen, kunnen scheikundigen en biologen voorspellen hoe biomoleculen zich in complexe systemen gedragen.
 Hoeveel waterstofatomen zijn er aan de linkerkant van de fotosynthese -vergelijking?
Hoeveel waterstofatomen zijn er aan de linkerkant van de fotosynthese -vergelijking?  Waaruit bestaat waterstof?
Waaruit bestaat waterstof?  Waarom is de grootte van een ion groter dan zijn ouderatoom?
Waarom is de grootte van een ion groter dan zijn ouderatoom?  Wanneer geplaatst in H2O, vangt een natriumpellet in brand als waterstofgas wordt bevrijd en hydroxide chemische of fysische verandering vormt?
Wanneer geplaatst in H2O, vangt een natriumpellet in brand als waterstofgas wordt bevrijd en hydroxide chemische of fysische verandering vormt?  Wat is de chemische formule van element neodymium?
Wat is de chemische formule van element neodymium?
Hoofdlijnen
- Wat gebruiken ze om cellen te zien?
- Welk enzym breekt cellulase af?
- Welk koninkrijk van organismen is het meest complex en waarom?
- Bemesting van de menselijke eiercel treedt meestal in wat voor?
- Welke theorie stelt dat alle cellen nieuwe cellen produceren?
- Multicellulaire eukaryoten die meestal mobiel zijn en voedsel verkrijgen van andere organismen behoren waarschijnlijk tot welk koninkrijk?
- Gefixeerd op eten?
- Wetenschappelijk onderbouwd slaapsuperfood:pompoenpitten
- Kan de wetenschap al onze vraag beantwoorden, heeft uw antwoord uitgelegd?
- Broze scheurgedrag begrijpen om sterkere materialen te ontwerpen

- Theoretische voorspelling van omgekeerde intersysteemkruising voor organische halfgeleiders

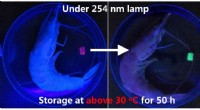
- Kunstmatig van kleur veranderend materiaal dat de huid van een kameleon nabootst, kan de versheid van zeevruchten detecteren
- Video:Wat is octaan eigenlijk?

- Chemische ingenieurs ontdekken manieren om vaste oppervlakken te modelleren om de interactie met water te verbeteren
 Wanneer een insect in barnsteen zit, is het een voorbeeld van welk type fossiel?
Wanneer een insect in barnsteen zit, is het een voorbeeld van welk type fossiel?  Wat zijn het representatieve organisme in herbivoor?
Wat zijn het representatieve organisme in herbivoor?  Business booming voor Braziliaanse boeren, maar ontbossing dreigt groot te worden
Business booming voor Braziliaanse boeren, maar ontbossing dreigt groot te worden Waarom is het kouder op het hoogtepunt van een berg?
Waarom is het kouder op het hoogtepunt van een berg?  Microreactor versnelt de productie van nanotech-deeltjes 500 keer
Microreactor versnelt de productie van nanotech-deeltjes 500 keer Berekening van de hydroniumionconcentratie op basis van de hydroxideconcentratie
Berekening van de hydroniumionconcentratie op basis van de hydroxideconcentratie  Is een mediaan accurater dan een gemiddelde?
Is een mediaan accurater dan een gemiddelde?  Hoe ziet de aarde eruit zonder water?
Hoe ziet de aarde eruit zonder water?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

