
Wetenschap
Waarom zilver niet reageert met verdund zwavelzuur:een chemische verklaring
Dit is waarom:
* De Reactiviteit-serie: Metalen zijn gerangschikt in een reactiviteitsreeks op basis van hun neiging om elektronen te verliezen en positieve ionen te vormen. Metalen hoger in de reeks zijn reactiever dan metalen lager in de reeks.
* De positie van waterstof: Waterstof wordt in de reactiviteitsreeks boven zilver geplaatst. Dit betekent dat waterstof reactiever is dan zilver.
* Reactiemechanisme: Wanneer een metaal reageert met een zuur, verliest het metaal elektronen en vormt het positieve ionen, terwijl de waterstofionen uit het zuur elektronen winnen en worden gereduceerd tot waterstofgas.
* Inactiviteit van Zilver: Omdat zilver minder reactief is dan waterstof, kan het geen waterstof uit het zwavelzuur verdringen. Dit betekent dat er geen waterstofgas ontstaat.
In plaats van te reageren met verdund zwavelzuur, reageert zilver met geconcentreerd zwavelzuur (heet) om zilversulfaat, zwaveldioxidegas en water te vormen. Deze reactie omvat de oxidatie van zilver en de reductie van zwavelzuur, wat leidt tot de vorming van deze producten.
Samenvattend verklaart de positie van zilver in de reactiviteitsreeks, lager dan waterstof, waarom het geen waterstofgas ontwikkelt bij reactie met verdund zwavelzuur.
 Impact van pH op reactiesnelheid:factoren en overwegingen
Impact van pH op reactiesnelheid:factoren en overwegingen  Welk type intermoleculaire kracht veroorzaakt de oplossing NaCl in water?
Welk type intermoleculaire kracht veroorzaakt de oplossing NaCl in water?  Identificeer het metaal dat wordt gebruikt als katalysator in Haber -proces?
Identificeer het metaal dat wordt gebruikt als katalysator in Haber -proces?  Nieuwe strategie voor isotopenscheiding met flexibel poreus materiaal
Nieuwe strategie voor isotopenscheiding met flexibel poreus materiaal Wetenschappers onderzoeken 3D-geprinte legeringen met hoge entropie
Wetenschappers onderzoeken 3D-geprinte legeringen met hoge entropie
 Waarom de Grote Meren geen getijden op oceaanschaal ervaren
Waarom de Grote Meren geen getijden op oceaanschaal ervaren  Wat gebeurt er met bladpigmenten als u ze water geeft met gekleurd water?
Wat gebeurt er met bladpigmenten als u ze water geeft met gekleurd water?  Als sneeuwvlokken, roetdeeltjes zijn uniek, klimaatmodellering beïnvloeden
Als sneeuwvlokken, roetdeeltjes zijn uniek, klimaatmodellering beïnvloeden Tsunami-veilige Golf is niets anders dan, experts waarschuwen
Tsunami-veilige Golf is niets anders dan, experts waarschuwen Wat is de naam van het eerste levende wezen op aarde?
Wat is de naam van het eerste levende wezen op aarde?
Hoofdlijnen
- Een protist die zijn eigen voedsel maakt, is een?
- Adaptieve straling:niet-voorbeelden en belangrijkste kenmerken identificeren
- Welk macromolecuul vormt een enzym?
- Fotosynthetische organismen halen hun koolstof uit?
- Wat voor soort gewervelde is de olifant?
- Waar wordt suiker geproduceerd in plantencellen?
- Leg uit met de wetenschap de acroniem wetenschap?
- Door UC geleid team laat zien hoe de bacteriële gemeenschap evolueert
- Wat is de reproductieve cyclus van bacteriën?
- Nieuwe methode zou kunnen helpen om zuiverder, veiligere medicijnen

- Krachtige nieuwe beeldvormingsmethode onthult in detail hoe deeltjes in oplossing bewegen
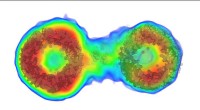
- Nieuwe methode voor het produceren van optische materialen verlaagt de kosten, verbetert de prestaties
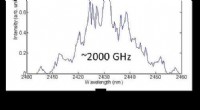
- Onderzoekers verbeteren de mechanische eigenschappen van aluminium/stalen verbindingen
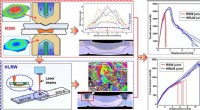
- Wetenschappers identificeren overgangsmetaal voor zeer efficiënte kooldioxide-activering
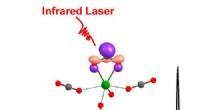
 Koolstofdioxide is een product van fotosynthese?
Koolstofdioxide is een product van fotosynthese?  Portland maakt vuile rivier schoon, nodigt bewoners uit om een duik te nemen
Portland maakt vuile rivier schoon, nodigt bewoners uit om een duik te nemen Welke landvormen vormen aardbevingen?
Welke landvormen vormen aardbevingen?  Onderzoekers rapporteren haptische interface voor mobiele technologie
Onderzoekers rapporteren haptische interface voor mobiele technologie Hoe fluor wordt gemaakt?
Hoe fluor wordt gemaakt?  Ben jij de directe afstammelingen van een uitheemse soort?
Ben jij de directe afstammelingen van een uitheemse soort?  Hybride apparaat oogst zowel mechanische als magnetische energie
Hybride apparaat oogst zowel mechanische als magnetische energie Onderzoekers creëren een snellere en goedkopere manier om kleine metalen structuren met licht te printen
Onderzoekers creëren een snellere en goedkopere manier om kleine metalen structuren met licht te printen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

