
Wetenschap
Methaan- en waterstofobligaties:het verschil begrijpen
Nee, methaan (CH4) bevat geen waterstofbrug.
Waterstofbruggen zijn een soort intermoleculaire kracht die optreedt tussen een waterstofatoom dat covalent gebonden is aan een zeer elektronegatief atoom (zoals zuurstof, stikstof of fluor) en een elektronenpaar in een naburig molecuul.
Methaan heeft alleen koolstof- en waterstofatomen. Koolstof is niet elektronegatief genoeg om een waterstofbrug te vormen, en de waterstofatomen zijn gebonden aan koolstof, niet aan een meer elektronegatief atoom.
Daarom interageren methaanmoleculen alleen via zwakkere Van der Waals-krachten, niet via waterstofbruggen.
 Waarom worden 18 groepselementen genaamd Noble Gases genaamd?
Waarom worden 18 groepselementen genaamd Noble Gases genaamd?  Waar komt stikstofoxide vandaan?
Waar komt stikstofoxide vandaan?  Wetenschappers onthullen verschillende substraatbindingsmodus in o-succinylbenzoyl-CoA-synthetase
Wetenschappers onthullen verschillende substraatbindingsmodus in o-succinylbenzoyl-CoA-synthetase De blauwe kleur in de kopersulfaatoplossing is te wijten aan de aanwezigheid van welk ionen?
De blauwe kleur in de kopersulfaatoplossing is te wijten aan de aanwezigheid van welk ionen?  Is water in een waterval gasvormig, vloeibaar of vast?
Is water in een waterval gasvormig, vloeibaar of vast?
Hoofdlijnen
- Ontdekking vergroot het begrip van hoe sommige virussen zich vermenigvuldigen
- Voorbeelden van organismen in het Archaebacteria -koninkrijk?
- Wetenschappers zetten primaten tegenover zoogdieren met kleinere hersenen om erachter te komen wie de slimste verzamelaar is
- Evolutie hoe werkt
- Wat zijn de twee soorten reproductie?
- Algen en meercellige planten zijn autotrofen omdat ze?
- Uit onderzoek blijkt dat planten droogtestresshormonen gebruiken om snackende spintmijten te blokkeren
- Hoe voeden schimmels zichzelf?
- Wat voor soort wetenschapper bestudeert Geass en bladeren?
- cel gedrag, ooit gehuld in mysterie, wordt geopenbaard in een nieuw licht

- Hoe wordt een metaal gevormd?
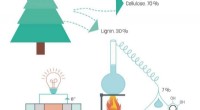
- Lignine – een supergroene brandstof voor brandstofcellen
- Onderzoekers onthullen op oxygenaat gebaseerde routes bij de omzetting van syngas via bifunctionele oxide-zeolietkatalysatoren

- Team zorgt voor stabiliteit van ontziltingsproces met magnesium

 Hoeveel bescherming is genoeg?
Hoeveel bescherming is genoeg?  Engel nummer 303:een mooie boodschap van vrede en persoonlijke groei
Engel nummer 303:een mooie boodschap van vrede en persoonlijke groei  Geologen en biologen ontdekken de atomaire vingerafdrukken van kanker
Geologen en biologen ontdekken de atomaire vingerafdrukken van kanker  NASA ziet aanhoudende overblijfselen van tropische cycloon 02W
NASA ziet aanhoudende overblijfselen van tropische cycloon 02W Hoe lagers werken
Hoe lagers werken  Waarom werd aluminium geplaatst waar het vandaag is op het periodieke tabel met elementen?
Waarom werd aluminium geplaatst waar het vandaag is op het periodieke tabel met elementen?  Hoe pond omzetten in Ounces
Hoe pond omzetten in Ounces  Hoe worden kristels van mineralen geclassificeerd?
Hoe worden kristels van mineralen geclassificeerd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

