
Wetenschap
Neutralisatiewarmte:HCl en NaOH uitgelegd - Chemie
Dit is waarom:
* Sterke zuren en basen dissociëren volledig in water. Dit betekent dat HCl en NaOH in oplossing voorkomen als respectievelijk H+- en Cl--ionen, en Na+- en OH--ionen.
* De neutralisatiereactie omvat hoofdzakelijk de vorming van water. Het H+-ion uit het zuur reageert met het OH-ion uit de base en vormt water (H2O):
H+ (aq) + OH- (aq) → H2O (l)
* De neutralisatiewarmte is de enthalpieverandering voor deze reactie. Omdat sterke zuren en basen volledig dissociëren, is de neutralisatiewarmte in wezen de enthalpieverandering voor de vorming van water uit zijn ionen, wat een constante waarde is.
Belangrijke opmerkingen:
*De neutralisatiewarmte kan enigszins variëren, afhankelijk van de specifieke concentraties van het gebruikte zuur en de base.
*Deze waarde van -57,3 kJ/mol geldt voor reacties onder standaardomstandigheden (298 K en 1 atm).
Laat het me weten als je nog vragen hebt.
 Welk type zure azijn bevat?
Welk type zure azijn bevat?  De toepassing van lineaire expansie in Engineering
De toepassing van lineaire expansie in Engineering Inzicht in scheidbare gem-Dimethylpieken in NMR-spectroscopie
Inzicht in scheidbare gem-Dimethylpieken in NMR-spectroscopie  ALLEEN DE PROTONEN DIE AAN KOOLSTOF GEBONDEN ZIJN, in volgorde van zuurgraad aflopend, de volgende verbindingen CH3CH2OH, CH3COCH3, CH3COH, CH3COOCH3?
ALLEEN DE PROTONEN DIE AAN KOOLSTOF GEBONDEN ZIJN, in volgorde van zuurgraad aflopend, de volgende verbindingen CH3CH2OH, CH3COCH3, CH3COH, CH3COOCH3?  Waarom heb je 40 gram calcium en 32 zwavel nodig om 72 sulfide te maken?
Waarom heb je 40 gram calcium en 32 zwavel nodig om 72 sulfide te maken?
Hoofdlijnen
- Hoe klimaatverandering planten onder druk zet en hun groei verandert
- Wat is de relatie tussen wetenschap en wetenschappelijke methode?
- Voorbeelden van archaebacteriën met hun wetenschappelijke naam en classificatie
- Wat is de naam van dikke wandvorm door bacteriecellen die wat kook- of bevriezingstemperatuur en ontsmettingsoplossingen kunnen overleven?
- Is lysosomen een prokaryotische of eukaryote -cel?
- Wat is één dierstructuur?
- Hoe bloemen zich aanpassen aan hun bestuivers
- De griezelige vraag van de vogelgriep:hoe miljoenen pluimvee te doden
- Waarom worden virussen niet opgenomen als onderdeel van de celtheorie?
- Slimme oplossing om bederf van zeevruchten op te sporen

- Waterstofproducerend enzym beschermt zichzelf tegen zuurstof

- Een nieuwe strategie om blauw licht te creëren uit een veelbelovend materiaal
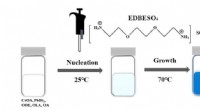
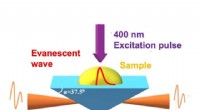
- Terahertz-golven onthullen verborgen processen in ultrasnelle kunstmatige fotosynthese
- ORNL bereikt belangrijke FDA-mijlpaal voor kankerbestrijdende Ac-225-isotoop
 Wat is de verbinding voor YCLO3?
Wat is de verbinding voor YCLO3?  Index -mineralen laten een wetenschapper 2 de geschiedenis van metamorfe rots begrijpen?
Index -mineralen laten een wetenschapper 2 de geschiedenis van metamorfe rots begrijpen?  Jumbo-kwal of enorme ster?
Jumbo-kwal of enorme ster?  Afbeelding:Lima, Peru gezien vanuit een baan om de aarde
Afbeelding:Lima, Peru gezien vanuit een baan om de aarde Hoe omgaan dieren met de dieren?
Hoe omgaan dieren met de dieren?  Hoe is het leven mogelijk bij hoge temperatuur?
Hoe is het leven mogelijk bij hoge temperatuur?  Gen-bewerkende baby's kunnen dodelijk zijn - maar sommige wetenschappers willen het toch doen
Gen-bewerkende baby's kunnen dodelijk zijn - maar sommige wetenschappers willen het toch doen  Wat waren de eerste organismen die zuurstof in de atmosfeer vrijgeven?
Wat waren de eerste organismen die zuurstof in de atmosfeer vrijgeven?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

