
Wetenschap
Natriumbisulfiet pH:inzicht in de zuurgraad en hydrolyse
Dit is waarom:
* Hydrolyse: Wanneer natriumbisulfiet oplost in water, ondergaat het hydrolyse, waarbij bisulfietionen (HSO₃⁻) en natriumionen (Na⁺) worden gevormd. De bisulfietionen kunnen een proton (H⁺) aan water doneren, waardoor de oplossing zuur wordt:
```
HSO₃⁻ + H₂O ⇌ SO₃²⁻ + H₃O⁺
```
* Evenwicht: Het evenwicht ligt aan de rechterkant, wat betekent dat meer bisulfietionen protonen doneren, waardoor de concentratie van hydroniumionen (H₃O⁺) toeneemt en de pH daalt.
Belangrijke opmerkingen:
* Concentratie: De exacte pH van een natriumbisulfietoplossing hangt af van de concentratie. Een meer geconcentreerde oplossing zal zuurder zijn.
* Temperatuur: Temperatuur heeft ook invloed op de pH. Een hogere temperatuur bevordert de productie van H₃O⁺, waardoor de oplossing zuurder wordt.
Laat het me weten als je nog vragen hebt!
 Een oceaan 13 miljoen jaar in de maak
Een oceaan 13 miljoen jaar in de maak Biochar kan op maat worden gemaakt voor een reeks milieuvoordelen, uit onderzoek blijkt
Biochar kan op maat worden gemaakt voor een reeks milieuvoordelen, uit onderzoek blijkt Wat is de betekenis van pad in relatie tot getijden en navigatie?
Wat is de betekenis van pad in relatie tot getijden en navigatie?  NASA meldt dat de aantasting van de ozonlaag in de Arctische stratosfeer in maart een recordniveau bereikte
NASA meldt dat de aantasting van de ozonlaag in de Arctische stratosfeer in maart een recordniveau bereikte Wat is familiezorg? Waarom het de voorkeur gaf aan Aboriginal-kinderen boven pleegkinderen
Wat is familiezorg? Waarom het de voorkeur gaf aan Aboriginal-kinderen boven pleegkinderen
Hoofdlijnen
- Hoe worden moleculen zoals eiwitten gedenatureerd?
- Waar classificeren wetenschappelijke namen organismen door?
- Wat is het oudste celtype?
- Kunnen vissen verkouden worden?
- Onthulling van de Triceratops-houding:een weinig bekend debat onthuld
- Waar in een embryo zijn de structuur die zich bevindt voor het bouwen van organen?
- Welke leeftijdsgroep heeft actieve enzymen?
- Hoe zijn zowel weefselorganen als orgaansystemen anders?
- Waarom hebben spiercellen meer mitochondriën dan enig ander celtype?
- Weg geopend om afval bij het opvangen van zonne-energie te minimaliseren
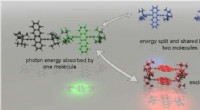
- Schimmel als geluidsabsorbeerder

- Moleculaire make-over maakt van slap antilichaam een SARS-CoV-2-tacker
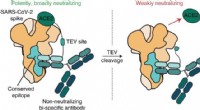
- Omkeerbare plakkerigheid in tandcement is iets om over te lachen
- Kunnen we kanker genezen door uit te zoeken hoe twee eiwitten op elkaar inwerken?

 Chilenen krijgen verkeerde tsunamiwaarschuwing na aardbeving op Antarctica
Chilenen krijgen verkeerde tsunamiwaarschuwing na aardbeving op Antarctica Intel lanceert derde patch voor strijd tegen MDS Goliath
Intel lanceert derde patch voor strijd tegen MDS Goliath Koolstofafvangproces produceert waterstof en bouwmaterialen
Koolstofafvangproces produceert waterstof en bouwmaterialen Uitspraak in MtGox bitcoin verduisteringszaak
Uitspraak in MtGox bitcoin verduisteringszaak Geen gletsjers, geen water?
Geen gletsjers, geen water? Hoeveel plaattektoniek zijn er?
Hoeveel plaattektoniek zijn er?  Hoe geleiding van warmte met behulp van de deeltjesheorie?
Hoe geleiding van warmte met behulp van de deeltjesheorie?  Wat zijn bodems die een goede afwatering hebben en gevormd op hoge breedtegraden geclassificeerd als?
Wat zijn bodems die een goede afwatering hebben en gevormd op hoge breedtegraden geclassificeerd als?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

