
Wetenschap
Ionische binding:valentie-elektronenoverdracht begrijpen
* Metalen hebben de neiging hun valentie-elektronen te verliezen om een stabiele elektronenconfiguratie te bereiken, meestal een octet (8 elektronen in de buitenste schil).
* Niet-metalen hebben de neiging om valentie-elektronen te verkrijgen om ook een stabiel octet te bereiken.
Zo werkt het:
1. Elektronenoverdracht: Wanneer een metaalatoom interageert met een niet-metaalatoom, *doneert* het metaalatoom zijn valentie-elektron(en) aan het niet-metaalatoom.
2. Vorming van ionen: Deze overdracht creëert twee tegengesteld geladen ionen:
* Het metaalatoom wordt een kation (positief geladen ion) omdat het elektronen heeft verloren.
* Het niet-metaalatoom wordt een anion (negatief geladen ion) omdat het elektronen heeft gewonnen.
3. Elektrostatische aantrekkingskracht: De sterke elektrostatische aantrekkingskracht tussen de tegengesteld geladen ionen houdt ze bij elkaar en vormt de ionische binding.
Voorbeeld:natriumchloride (NaCl)
* Natrium (Na) heeft 1 valentie-elektron. Het verliest dit elektron en wordt een natriumkation (Na+).
* Chloor (Cl) heeft 7 valentie-elektronen. Het krijgt één elektron om een chloride-anion (Cl-) te worden.
*De tegengesteld geladen ionen (Na+ en Cl-) worden bij elkaar gehouden door de elektrostatische aantrekking, waardoor de ionische verbinding natriumchloride ontstaat.
Belangrijkste punten:
* Ionische bindingen omvatten de volledige overdracht van valentie-elektronen, niet het delen ervan.
* De resulterende ionen hebben een stabiele elektronenconfiguratie, meestal een octet.
*De sterke elektrostatische aantrekkingskracht tussen de ionen is de drijvende kracht achter de binding.
 Welke 4 ingrediënten zijn door een plant nodig om fotosynthese uit te voeren?
Welke 4 ingrediënten zijn door een plant nodig om fotosynthese uit te voeren?  Hoe om te zien of iets polair of niet-polair is
Hoe om te zien of iets polair of niet-polair is  Het element dat in elke ORGANISCHE verbinding aanwezig is, is?
Het element dat in elke ORGANISCHE verbinding aanwezig is, is?  Waarom heeft fluor een kleinere atoomstraal dan zowel zuurstof als chloor?
Waarom heeft fluor een kleinere atoomstraal dan zowel zuurstof als chloor?  Welk sap zal het snelst verdampen met zout?
Welk sap zal het snelst verdampen met zout?
 Nieuw model van de mariene zwavelcyclus na de ijstijd van de sneeuwbalaarde
Nieuw model van de mariene zwavelcyclus na de ijstijd van de sneeuwbalaarde De limiet dat bomen niet voorbij een berg groeien?
De limiet dat bomen niet voorbij een berg groeien?  De gevaren van aluminiumfolie
De gevaren van aluminiumfolie  Deze sociale wetenschap houdt zich bezig met hoe cultuur van generatie is doorgegeven, terwijl mensen veranderingen in milieutechnologie of verandering aanpassen. Zouden S?
Deze sociale wetenschap houdt zich bezig met hoe cultuur van generatie is doorgegeven, terwijl mensen veranderingen in milieutechnologie of verandering aanpassen. Zouden S?  Te schattig om te doden? Amerikaanse verdeeldheid over herten in de voorsteden
Te schattig om te doden? Amerikaanse verdeeldheid over herten in de voorsteden
Hoofdlijnen
- Een tabel maken waarin de reproductieve structuren processen van Zygote Fungi Sac Club -schimmels vergelijken en contrasteren?
- Welke moleculen fungeren als energieopslagmolecuul in de spieren door fosfor te doneren om ATP en ADP opnieuw te synthetiseren?
- Een botabsorberende cel wordt een genoemd?
- Welke genen maakt geen deel uit van het lac -operon?
- Wat is apoptose?
- Wat voert veel verschillende banen in de cel uit?
- Welke wetenschappers gebruiken de wetenschappelijke methode?
- Wat voor soort dier eet een alomtegenwoordig?
- Wat is de waarschijnlijke bron van organisme die het beste groeit met Celsius van 37 graden?
- Nieuw polymeer verbetert het vermogen van tribo-elektrische nanogeneratoren

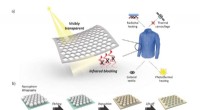
- Nieuwe nanofotonische coating kan bijdragen aan thermisch beheer en contra-surveillance
- Een kijkje op dun ijs

- Video:De toevallige ontdekking van LSD

- Water helpt bij de onverwachte en ultrasnelle synthese van collageenachtig synthetisch poly-L-proline

 Kunnen heliumatomen worden opgesplitst in twee waterstofatomen?
Kunnen heliumatomen worden opgesplitst in twee waterstofatomen?  Hoe detectielimiet van detectie (LOD) te berekenen
Hoe detectielimiet van detectie (LOD) te berekenen  Wat is de functie van een embryo in een ei?
Wat is de functie van een embryo in een ei?  Een cursief maken F
Een cursief maken F  Hoe beschrijf je het cytoplasma?
Hoe beschrijf je het cytoplasma?  Waarom is de energiestroom in een ecosysteem beschreven als één manier?
Waarom is de energiestroom in een ecosysteem beschreven als één manier?  Wat zijn voorbeelden van oplosbare vaste stoffen?
Wat zijn voorbeelden van oplosbare vaste stoffen?  Earth Day Leuke weetjes voor kinderen
Earth Day Leuke weetjes voor kinderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

