
Wetenschap
Valentie en reactiviteit:elementen vergelijken met 7 en 8 valentie-elektronen
* Octetregel: Atomen streven naar een stabiele elektronenconfiguratie zoals de edelgassen, die een volledige buitenschil hebben (8 valentie-elektronen).
* Reactiviteit: Elementen met 7 valentie-elektronen zijn slechts één elektron verwijderd van het bereiken van een volledig octet. Dit maakt ze zeer reactief omdat ze gemakkelijk een elektron verkrijgen om hun buitenste schil te voltooien.
* Voorbeeld: Halogenen (zoals chloor, fluor, broom) bevinden zich in groep 17 van het periodiek systeem en hebben 7 valentie-elektronen. Het zijn zeer reactieve niet-metalen.
* Stabiliteit: Elementen met 8 valentie-elektronen hebben een volledige buitenschil en zijn zeer stabiel, wat betekent dat ze niet reactief zijn. Dit is de reden waarom edelgassen inert zijn.
Samenvattend zijn elementen met 7 valentie-elektronen zeer reactief omdat ze één elektron verwijderd zijn van het bereiken van een stabiel octet, terwijl elementen met 8 valentie-elektronen al stabiel en niet-reactief zijn.
 Hoeveel mol CO2 worden geproduceerd uit elke mol C2H5OH volledig verbrand?
Hoeveel mol CO2 worden geproduceerd uit elke mol C2H5OH volledig verbrand?  Wat is het effect van mierenzuur verdund met water?
Wat is het effect van mierenzuur verdund met water?  Welke verklaring beschrijft het beste de tweede wet van de thermodynamica?
Welke verklaring beschrijft het beste de tweede wet van de thermodynamica?  De formule van de verbinding vormde zich wanneer aluminium en chloorbinding?
De formule van de verbinding vormde zich wanneer aluminium en chloorbinding?  Is korst een vaste vloeistof of gas?
Is korst een vaste vloeistof of gas?
 Trias biostratigrafie, lithostratigrafie en paleogeografie van het Qinghai-Tibetaanse plateau
Trias biostratigrafie, lithostratigrafie en paleogeografie van het Qinghai-Tibetaanse plateau  Hevige tyfoon Doksuri bestormt centraal Vietnam
Hevige tyfoon Doksuri bestormt centraal Vietnam Opinie:waarom Amerikaanse bedrijven de terugtrekking van Trump uit het klimaatakkoord van Parijs negeren
Opinie:waarom Amerikaanse bedrijven de terugtrekking van Trump uit het klimaatakkoord van Parijs negeren Wat is het temperatuurbereik binnen de asteriosfeer?
Wat is het temperatuurbereik binnen de asteriosfeer?  Welke soorten vlooien leven in Florida?
Welke soorten vlooien leven in Florida?
Hoofdlijnen
- De giftige suikerboom:de evolutionaire geschiedenis van een kankerachtig suikergen in kaart brengen
- 3 weefsels die het vasculaire systeem vormen in een zaadplant?
- Waar kan men informatie vinden over hele genoomsequencing?
- Hoe beschrijf je de evolutietheorie door natuurlijke selectie?
- Hoe libellen zichzelf oprichten als ze ondersteboven worden neergezet
- Een geheim wapen voor muggen:een lichte aanraking en sterke vleugels
- Herstel van iconische inheemse vogel veroorzaakt problemen in stedelijke gebieden
- Hoe is celdeling belangrijk voor een single -organisme?
- Wat is een nimf in de wetenschap?
- Bacteriële hechting in vitro en in silico
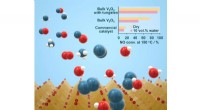
- Door wolfraam vervangen vanadiumoxide ademt frisse lucht in de katalysatortechnologie
- Verschillen in vetweefsel lichtreflecterende eigenschappen zorgen voor gemakkelijke detectie

- Zeer selectieve terugwinning van lanthaniden via gelaagd vanadaat met zuur- en stralingsbestendigheid

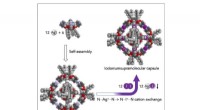
- Een nieuwe hexamere moleculaire capsule van nanoformaat
 Wat is een estherosfeer?
Wat is een estherosfeer?  NASA vindt potentieel voor zware regenval in nieuwe tropische cycloon Pola
NASA vindt potentieel voor zware regenval in nieuwe tropische cycloon Pola Wat zijn enkele redenen voor dichtheidsfouten?
Wat zijn enkele redenen voor dichtheidsfouten?  Wat is de temperatuur op Fahrenheit -schaal waarbij alle moleculaire beweging vrijwel stopt?
Wat is de temperatuur op Fahrenheit -schaal waarbij alle moleculaire beweging vrijwel stopt?  Hoe ziet zonne -energie eruit?
Hoe ziet zonne -energie eruit?  Kanker op nanoschaal aanpakken
Kanker op nanoschaal aanpakken  Welk type energie gebruikt een vaatwasser?
Welk type energie gebruikt een vaatwasser?  Wie ontdekte Atomic Orbital?
Wie ontdekte Atomic Orbital?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

