
Wetenschap
Chemische vergelijkingen begrijpen:een gids voor beginners
Componenten van een chemische vergelijking:
1. Reactanten: De stoffen die aan het begin van de reactie aanwezig zijn en transformatie ondergaan. Ze staan aan de linkerkant van de vergelijking.
2. Producten: De stoffen die zijn gevormd als gevolg van de reactie. Ze staan aan de rechterkant van de vergelijking.
3. Pijl: Een symbool dat de reactanten en producten van elkaar scheidt en de richting van de reactie aangeeft. Het wijst meestal van links naar rechts en laat zien hoe de reactanten in producten transformeren.
4. Coëfficiënten: Getallen geplaatst voor elke chemische formule. Ze vertegenwoordigen het relatieve aantal mol van elke stof die bij de reactie betrokken is. Deze coëfficiënten zorgen ervoor dat de vergelijking in evenwicht is, wat betekent dat hetzelfde aantal atomen van elk element aan beide kanten van de vergelijking aanwezig is.
5. Fysieke toestanden: Soms wordt de fysieke toestand van elke stof aangegeven met haakjes:(s) voor vaste stof, (l) voor vloeistof, (g) voor gas en (aq) voor waterige oplossing.
Voorbeeld:
De reactie van waterstofgas met zuurstofgas om water te vormen kan worden weergegeven door de volgende vergelijking:
2H₂(g) + O₂(g) → 2H₂O(l)
Uitleg:
* Reactanten: Waterstofgas (H₂) en zuurstofgas (O₂)
* Producten: Water (H₂O)
* Pijl: → geeft de vorming van producten uit reactanten aan.
* Coëfficiënten: 2 vóór H₂ en H₂O brengt de vergelijking in evenwicht door ervoor te zorgen dat er aan beide zijden vier waterstofatomen en twee zuurstofatomen aanwezig zijn.
Belangrijkste punten:
* Chemische vergelijkingen zijn een beknopte en universele manier om chemische reacties weer te geven.
* Ze geven informatie over de reactanten, producten en stoichiometrie (de relatieve hoeveelheden betrokken stoffen).
* Het in evenwicht brengen van chemische vergelijkingen is van cruciaal belang om ervoor te zorgen dat de wet van behoud van massa wordt nageleefd.
Meer dan basisweergave:
* Reactieomstandigheden: Soms worden specifieke omstandigheden zoals temperatuur, druk of de aanwezigheid van een katalysator boven of onder de pijl aangegeven.
* Reactiemechanismen: Voor complexe reacties gebruiken wetenschappers gedetailleerde mechanismen om de individuele stappen weer te geven die bij de totale reactie betrokken zijn.
* Thermochemische vergelijkingen: Deze omvatten enthalpieverandering (ΔH) om aan te geven of bij een reactie warmte vrijkomt of absorbeert.
Het begrijpen van chemische vergelijkingen is van fundamenteel belang in de scheikunde. Ze stellen wetenschappers in staat de uitkomsten van reacties te voorspellen, hoeveelheden reactanten en producten te berekenen en de onderliggende principes van chemische transformaties te onderzoeken.
 Wat is de gebalanceerde vergelijking die de reactie beschrijft tussen waterstofgas en stikstof om ammoniak NH3 te produceren?
Wat is de gebalanceerde vergelijking die de reactie beschrijft tussen waterstofgas en stikstof om ammoniak NH3 te produceren?  Waarom macrofagen rusten in gezond weefsel?
Waarom macrofagen rusten in gezond weefsel? Een verbinding samengesteld uit koolstofwaterstof en zuurstof met drie vetzuren bevestigd aan een molecuul glycerol is?
Een verbinding samengesteld uit koolstofwaterstof en zuurstof met drie vetzuren bevestigd aan een molecuul glycerol is?  Verandert het oplossen van een suikerkubus in kopje chemische kopje chemische kop?
Verandert het oplossen van een suikerkubus in kopje chemische kopje chemische kop?  1000 mg NaCl gelijk hoeveel zout?
1000 mg NaCl gelijk hoeveel zout?
 Rivieren smelten poolijs, opwarmende lucht en oceaan
Rivieren smelten poolijs, opwarmende lucht en oceaan Wat gebeurt er als een orkaan optreedt?
Wat gebeurt er als een orkaan optreedt?  Noordelijke veengebieden bevatten mogelijk twee keer zoveel koolstof als eerder werd gedacht
Noordelijke veengebieden bevatten mogelijk twee keer zoveel koolstof als eerder werd gedacht Draagt koude natuurbrandrook bij aan waterafstotende bodems in verbrande gebieden?
Draagt koude natuurbrandrook bij aan waterafstotende bodems in verbrande gebieden? Bredere dekking van satellietgegevens detecteert de aanvoer van magma naar vulkanen beter
Bredere dekking van satellietgegevens detecteert de aanvoer van magma naar vulkanen beter
Hoofdlijnen
- Biologen ontdekken genetische routes die het immuunsysteem en de bloedsomloop van muggen tijdens infectie met elkaar verbinden
- Zijn de cellen die water verplaatsen in planten xyleem of floëemscheep niet?
- In welk type cellen komt prokaryoten en eukaryoten de celcyclus op?
- Gregor Mendel - Vader van genetica: biografie, experimenten en feiten
- Cellen in de bladeren van planten bevatten gespecialiseerde structuren die chloroplasten worden genoemd, hoe zijn gerelateerd aan functiebladcellen?
- Waar zou je een cel vinden die een groot aantal chloroplasten bevatte?
- Welk deel van de dierencel dat de plant niet heeft?
- Meeldauw versus schimmel:wat is het verschil?
- Waarom vormen wetenschappers een hypothese?
- De smaak behouden, het verminderen van het zout

- Metaaloplossing:een chemische eigenschap uitgelegd

- Oneindig recyclebaar polymeer toont praktische eigenschappen van kunststoffen

- Strategie suggereert manieren om zich voor te bereiden op opkomende antibioticaresistente superbacteriën

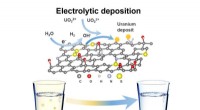
- Grafeenschuim gebruiken om gifstoffen uit drinkwater te filteren
 Hoe heet is de koffie van Schrödinger?
Hoe heet is de koffie van Schrödinger?  Wat is perineurium?
Wat is perineurium?  Extreem weer wordt steeds extremer
Extreem weer wordt steeds extremer Hoe worden de golven genoemd die meer energie hebben dan licht die je kunt zien?
Hoe worden de golven genoemd die meer energie hebben dan licht die je kunt zien?  Egg Drop Device Ideas
Egg Drop Device Ideas  Kan een versnellend object een snelheid van nul hebben?
Kan een versnellend object een snelheid van nul hebben?  Wat zijn de mijlpalen in Human Genome Project van 1983-2008?
Wat zijn de mijlpalen in Human Genome Project van 1983-2008?  Benoemde, hoeveel atomen komen op natuurlijke wijze voor?
Benoemde, hoeveel atomen komen op natuurlijke wijze voor?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

