
Wetenschap
Inzicht in de krachten die vloeibare stikstof bij elkaar houden
Hier is een overzicht:
* Stikstof is een niet-polair molecuul: Stikstofgas (N2) bestaat uit twee stikstofatomen die drievoudig aan elkaar gebonden zijn. Deze sterke binding creëert een symmetrisch molecuul zonder permanent dipoolmoment.
* Van der Waals krachten: Dit zijn zwakke, tijdelijke aantrekkingskrachten die voortkomen uit de constante beweging van elektronen in moleculen.
* Verspreidingskrachten in Londen: Dit zijn de zwakste soorten van der Waals-krachten, die optreden tussen alle moleculen, zelfs niet-polaire. Ze ontstaan uit tijdelijke, onmiddellijke dipolen die in de elektronenwolken van moleculen worden geïnduceerd als gevolg van de willekeurige beweging van elektronen.
Hoe het werkt:
1. Tijdelijke dipolen: Terwijl elektronen rond het stikstofmolecuul bewegen, kunnen ze vluchtige momenten creëren waarin het ene uiteinde van het molecuul iets negatiever wordt en het andere uiteinde iets positiever.
2. Attractie: Deze tijdelijke dipolen induceren tijdelijke dipolen in aangrenzende stikstofmoleculen. De tegengestelde ladingen van deze tijdelijke dipolen trekken elkaar vervolgens aan en houden de moleculen bij elkaar.
Belangrijke punten:
* Zwakke krachten: Hoewel deze krachten afzonderlijk zwak zijn, is het cumulatieve effect van veel Londense dispersiekrachten voldoende om vloeibare stikstof bij lage temperaturen bij elkaar te houden.
* Laag kookpunt: De zwakte van deze krachten verklaart waarom stikstof een zeer laag kookpunt heeft (-195,8 °C) - de thermische energie bij hogere temperaturen overwint de krachten die de vloeistof bij elkaar houden.
Samengevat: Vloeibare stikstof wordt bij elkaar gehouden door tijdelijke, zwakke aantrekkingskrachten die bekend staan als London-dispersiekrachten, die voortkomen uit de tijdelijke dipolen die worden geïnduceerd in de elektronenwolken van stikstofmoleculen als gevolg van willekeurige elektronenbeweging.
 Welk voorbeeld van slechte geleider warmtematerialen?
Welk voorbeeld van slechte geleider warmtematerialen?  Beschrijf twee manieren waarop radioactieve isotopen worden gebruikt in biomedisch onderzoek?
Beschrijf twee manieren waarop radioactieve isotopen worden gebruikt in biomedisch onderzoek?  Vullen deeltjes in een gas de bodem van hun containers ongeacht de vorm- of volumecontainer?
Vullen deeltjes in een gas de bodem van hun containers ongeacht de vorm- of volumecontainer?  Hoe om te zien of iets polair of niet-polair is
Hoe om te zien of iets polair of niet-polair is  Welk reagens u gebruikt om aniline om te zetten in chloorbenzeen?
Welk reagens u gebruikt om aniline om te zetten in chloorbenzeen?
 Zonlicht kan zeeplastic afbreken tot tienduizenden chemische verbindingen
Zonlicht kan zeeplastic afbreken tot tienduizenden chemische verbindingen Wat is een effect van natuurlijke selectie?
Wat is een effect van natuurlijke selectie?  Politieke voorkeur beïnvloedt het waterbeleid van de stad even sterk als het klimaat
Politieke voorkeur beïnvloedt het waterbeleid van de stad even sterk als het klimaat Uitgebreid overzicht van klimaatschommelingen in het verleden nu beschikbaar dankzij laserbeeldvorming van schelpen
Uitgebreid overzicht van klimaatschommelingen in het verleden nu beschikbaar dankzij laserbeeldvorming van schelpen Wil je het leven vinden? Vergelijk een planeet met zijn buren
Wil je het leven vinden? Vergelijk een planeet met zijn buren
Hoofdlijnen
- De embryonale oorsprong van al het neurale weefsel?
- Wat is de betekenis van antropogeen?
- Wat is een katabole route waarin organische moleculen worden afgebroken om energie vrij te maken voor gebruik door de cel?
- Ontdekt? Nieuw maar uitgestorven menselijk familielid uit Melanesië
- Wat is de ruimte in een cel die voedselwater enzymen of afval opslaat?
- Het verschil tussen prokaryotische en eukaryotische genexpressie
- Wat gedraagt zich als een kern in de cel?
- Waarom wordt een pridictie gebruikt bij wetenschappelijke expermentatie?
- Welke aanpassingen zitten er in een spinnenplant?
- Gebruik van smeltpolymerisatie om robuust covalent organisch raamwerkschuim te fabriceren
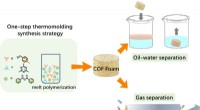
- Nieuw geavanceerd materiaal vertoont buitengewone stabiliteit over een breed temperatuurbereik

- Lab op een chip kan gezondheid monitoren, ziektekiemen en verontreinigende stoffen

- Team onthult katalysator die problematische CF-bindingen kan verbreken
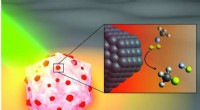
- Moleculaire bindingen smeden met groen licht

 Wat is de staat van materie Mercurius in vloeistof?
Wat is de staat van materie Mercurius in vloeistof?  Wie heeft vrije cel ontdekt en nucleus waargenomen?
Wie heeft vrije cel ontdekt en nucleus waargenomen?  Zijn de mineralen gedolven in Noord -Kaap hernieuwbaar?
Zijn de mineralen gedolven in Noord -Kaap hernieuwbaar?  Groen licht voor een nieuwe generatie dynamische materialen
Groen licht voor een nieuwe generatie dynamische materialen Computationele strategieën overwinnen obstakels bij de ontwikkeling van peptidetherapieën
Computationele strategieën overwinnen obstakels bij de ontwikkeling van peptidetherapieën Hoe veranderen zonnepanelen de stralen in elektriciteit?
Hoe veranderen zonnepanelen de stralen in elektriciteit?  Hartslagsensoren op afstand kunnen worden beïnvloed door een donkere huid. UCLA-team biedt oplossing
Hartslagsensoren op afstand kunnen worden beïnvloed door een donkere huid. UCLA-team biedt oplossing Bijna-religieuze marketing-ijver houdt de smartphonewereld in zijn greep
Bijna-religieuze marketing-ijver houdt de smartphonewereld in zijn greep
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

