
Wetenschap
Ionische verbindingen:formules en structuur begrijpen
* Ionische binding: Ionische verbindingen worden gevormd door de elektrostatische aantrekking tussen positief geladen ionen (kationen) en negatief geladen ionen (anionen). Ze vormen geen afzonderlijke moleculen zoals covalente verbindingen dat doen.
* Roosterstructuur: In plaats van moleculen bestaan ionische verbindingen als uitgebreide driedimensionale roosters. In deze structuur zijn ionen gerangschikt in een regelmatig, herhalend patroon.
* Empirische formule: Ionische verbindingen worden weergegeven door hun empirische formule , die de eenvoudigste gehele getalsverhouding van de aanwezige ionen toont. Deze formule weerspiegelt de verhouding van ionen in het rooster, niet de samenstelling van individuele moleculen.
Voorbeeld:
* Natriumchloride (NaCl): De empirische formule vertegenwoordigt één natriumion (Na+) voor elk chloride-ion (Cl-) in het kristalrooster. Er is geen duidelijk 'NaCl-molecuul'.
Samengevat: Ionische verbindingen hebben geen moleculaire formules omdat ze niet als afzonderlijke moleculen bestaan, maar als uitgebreide roosters van ionen. Hun samenstelling wordt weergegeven door empirische formules, die de eenvoudigste gehele getalsverhouding van ionen in het rooster aangeven.
 Hoe lichtdeeltjes druppels de perfecte vloeistof kunnen produceren
Hoe lichtdeeltjes druppels de perfecte vloeistof kunnen produceren  65 ml hcl wordt getitreerd met een oplossing van 0,15 m koh. Er zijn 44 nodig om het equivalentiepunt te bereiken. Welke concentratie oplossing?
65 ml hcl wordt getitreerd met een oplossing van 0,15 m koh. Er zijn 44 nodig om het equivalentiepunt te bereiken. Welke concentratie oplossing?  Hoeveel elektronen zijn cadeautjes in fluoratoom?
Hoeveel elektronen zijn cadeautjes in fluoratoom?  Hoe ziet ethyleendiaminetetraaceticzuur eruit?
Hoe ziet ethyleendiaminetetraaceticzuur eruit?  Hoe verschillen ijswatermoleculen van warme moleculen?
Hoe verschillen ijswatermoleculen van warme moleculen?
 Bezuinigingen op luchtvervuiling redden levens in de staat New York
Bezuinigingen op luchtvervuiling redden levens in de staat New York Inzicht in kwikdamplampen en -balans
Inzicht in kwikdamplampen en -balans Wetenschappers schatten de ijsdikte en subglaciale terreinen in de Yulong-sneeuwberg
Wetenschappers schatten de ijsdikte en subglaciale terreinen in de Yulong-sneeuwberg Vervuilen wetenschappers hun eigen monsters met microvezels?
Vervuilen wetenschappers hun eigen monsters met microvezels? Op een afgelegen eiland, een verloren deel van de wereld is gevonden
Op een afgelegen eiland, een verloren deel van de wereld is gevonden
Hoofdlijnen
- Wat is alumanodi?
- Onderzoek toont aan hoe hongerige bacteriën voedingsstoffen in hun omgeving waarnemen
- Welke dingen hebben dierencellen die plant niet?
- Wat is de langste fase van de celcyclus?
- Wat is een unieke rol van organismen in het ecosysteem?
- Waarom is de vorm van eiwitmoleculen belangrijk?
- Wat zijn de verschillen van eenvoudig en gestratificeerd weefsel?
- Gebruiken alle vormen van leven aminozuren in DNA om genetische informatie op te slaan?
- Vraag ons het type bioloog meestal werkt in binnenlaboratoria?
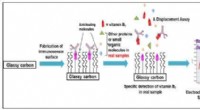
- Vitamine B7-bewakingsapparaat voor analyse van voedsel en klinische monsters
- Innovatieve combinatie van harde en zachte materialen verbetert de hechting op ruwe oppervlakken

- Hoe valentie-elektronen de atoomstraal van een element vormen

- Gifbestrijding:op jacht naar het tegengif
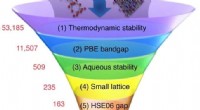
- Uitgebreide elektronische structuurmethoden voor materiaalontwerp
 Het celmembraan en de nucleaire zijn gemaakt?
Het celmembraan en de nucleaire zijn gemaakt?  Nederlands-Chinese radiotelescoopantennes ontvouwen achter de maan
Nederlands-Chinese radiotelescoopantennes ontvouwen achter de maan Cefalisatie wordt geassocieerd met welk systeem?
Cefalisatie wordt geassocieerd met welk systeem?  Nieuw model heeft tot doel het gebrek aan miniatuur zwarte gaten in het vroege heelal te verklaren
Nieuw model heeft tot doel het gebrek aan miniatuur zwarte gaten in het vroege heelal te verklaren  Waar is Calvary Hill nu gelegen op welke Jezus Christus stierf?
Waar is Calvary Hill nu gelegen op welke Jezus Christus stierf?  Welk idee van gebaseerd op fossiel en de moderne organismen die hij in feite heeft gevonden, zegt in feite dat genetische veranderingen door latere generaties worden geërfd?
Welk idee van gebaseerd op fossiel en de moderne organismen die hij in feite heeft gevonden, zegt in feite dat genetische veranderingen door latere generaties worden geërfd?  Wat is de hoeveelheid kracht waarmee de zwaartekracht iets naar beneden trekt?
Wat is de hoeveelheid kracht waarmee de zwaartekracht iets naar beneden trekt?  Google CEO zegt belangrijk om China-project te verkennen
Google CEO zegt belangrijk om China-project te verkennen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

