
Wetenschap
Neutralisatie van HCl en NaOH:concentratieveranderingen begrijpen
* Neutralisatiereactie: De reactie tussen HCl (een sterk zuur) en NaOH (een sterke base) is een neutralisatiereactie. De vergelijking is:
HCl (aq) + NaOH (aq) → NaCl (aq) + H₂O (l)
* Verbruik van reactanten: Bij de reactie worden zowel HCl als NaOH verbruikt en deze omgezet in natriumchloride (NaCl) en water (H₂O).
* Afnemende HCl-concentratie: Naarmate de reactie vordert, neemt de hoeveelheid HCl in de oplossing af, wat leidt tot een lagere concentratie.
* Volledige neutralisatie: Wanneer de reactie een punt bereikt waarop alle HCl met NaOH heeft gereageerd, wordt gezegd dat de oplossing is geneutraliseerd. Op dit punt zou de concentratie HCl feitelijk nul zijn.
Belangrijke opmerking: De uiteindelijke concentratie van de oplossing hangt af van de initiële concentraties van HCl en NaOH en de stoichiometrie van de reactie.
 Wat is een sterkere base Ammoniak of natriumhydroxide?
Wat is een sterkere base Ammoniak of natriumhydroxide?  Wat is het radioactieve materiaal in kernwapens?
Wat is het radioactieve materiaal in kernwapens?  Wat zijn fysieke eigenschappen van bitumen?
Wat zijn fysieke eigenschappen van bitumen?  Wat wordt gevormd in de atmosfeer wanneer chemicaliën die vluchtige organische verbinding worden genoemd en stikstofdioxide worden uitgevoerd door zonlicht?
Wat wordt gevormd in de atmosfeer wanneer chemicaliën die vluchtige organische verbinding worden genoemd en stikstofdioxide worden uitgevoerd door zonlicht?  Waarom is de gaszwavel hexafluoride zwaarder dan lucht?
Waarom is de gaszwavel hexafluoride zwaarder dan lucht?
 Hoe was de aarde op het moment dat er maar één organisme is?
Hoe was de aarde op het moment dat er maar één organisme is?  Nieuwe vulkanische lavaspleet in Hawaï zorgt voor meer evacuaties
Nieuwe vulkanische lavaspleet in Hawaï zorgt voor meer evacuaties UN World Ocean Assessment:de oceaan heeft problemen, maar we hebben nog tijd om te handelen
UN World Ocean Assessment:de oceaan heeft problemen, maar we hebben nog tijd om te handelen Werken tussen de pinguïns? Frankrijk zoekt kandidaten
Werken tussen de pinguïns? Frankrijk zoekt kandidaten Waarom is het meeste water in de atmosfeer onzichtbaar?
Waarom is het meeste water in de atmosfeer onzichtbaar?
Hoofdlijnen
- Waarom is het belangrijk voor cellen van meercellige organismen om mitose te ondergaan?
- Nieuwe soorten mariene spin verschijnen bij eb om wetenschappers aan Bob Marley te herinneren
- Het perengenoom kraken:hoe studenten hielpen een nieuw hulpmiddel voor de industrie te ontsluiten
- Structuren gevonden in protoplasma om cellen te helpen functioneren?
- Enzymen kunnen de sleutel zijn om te begrijpen hoe DNA muteert, vinden kwantumbiologen
- Wat zijn de twee hoofdfasen in de synthese van eiwitten en waar komt elk voor?
- Spelt of zachte tarwe? Hun diversiteit aan voedingscomponenten verhindert de identificatie welke soort gezonder is
- Hoe planten tomatenplanten zich voort?
- Nieuwe studie laat zien hoe het Ebola-virus cellen infecteert
- Een nucleair ongeval met vermalen mineralen bevatten

- Een nieuw magnetisch materiaal en opnameproces om de datacapaciteit enorm te vergroten

- Dampdruk omzetten in gasconcentratie:een praktische gids

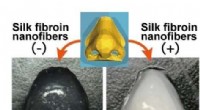
- Zijdevezels verbeteren bioinkt voor 3D-geprinte kunstmatige weefsels en organen
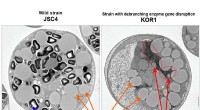
- Koolhydraten omzetten in lipiden voor biobrandstoffen voor microalgen
 Kleine satellieten zijn van vitaal belang voor de Australische ruimtevaartindustrie - en ze zullen geen ruimteafval zijn
Kleine satellieten zijn van vitaal belang voor de Australische ruimtevaartindustrie - en ze zullen geen ruimteafval zijn Hoe worden de elementen Li en Fe gemaakt?
Hoe worden de elementen Li en Fe gemaakt?  Hoe helpt uitdroging bacteriën onder controle te houden?
Hoe helpt uitdroging bacteriën onder controle te houden?  Een siliconen beeldsensor die rekent
Een siliconen beeldsensor die rekent Hoe stelt u de krachtrichting vast die wordt uitgeoefend op glas?
Hoe stelt u de krachtrichting vast die wordt uitgeoefend op glas?  Wat is de totale elektrische lading op moleculen en verbindingen?
Wat is de totale elektrische lading op moleculen en verbindingen?  EPA stelt definitieve beslissing over transparantieregel voor wetenschap uit
EPA stelt definitieve beslissing over transparantieregel voor wetenschap uit Schaal van online schade aan kinderen onthuld in mondiaal onderzoek
Schaal van online schade aan kinderen onthuld in mondiaal onderzoek
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

