
Wetenschap
Inzicht in de relatie tussen pH en hydroniumionconcentratie
* pH-schaal: De pH-schaal meet de zuurgraad of alkaliteit van een oplossing. Het varieert van 0 tot 14, met:
* 0 tot 6,9: Zure oplossingen (hogere H₃O⁺-concentratie)
* 7: Neutrale oplossing (gelijke H₃O⁺- en OH⁻-concentratie)
* 7.1 tot 14: Basische of alkalische oplossingen (lagere H₃O⁺-concentratie)
* De relatie: De pH wordt berekend met behulp van de volgende vergelijking:
pH =-log[H₃O⁺]
waarbij [H₃O⁺] de concentratie hydroniumionen in mol per liter (M) vertegenwoordigt.
* Belangrijkste punten:
* Naarmate de concentratie hydroniumionen toeneemt , de pH neemt af (zuurder).
* Naarmate de concentratie hydroniumionen afneemt , de pH neemt toe (meer alkalisch).
Voorbeeld:
* Een oplossing met een hydroniumionconcentratie van 1 x 10⁻⁴ M heeft een pH van 4.
* Een oplossing met een hydroniumionconcentratie van 1 x 10⁻¹⁰ M heeft een pH van 10.
Samengevat:
* Hoger [H₃O⁺] =Lagere pH (zuurrijker)
* Lager [H₃O⁺] =Hogere pH (meer alkalisch)
 Kooldioxide transformeren - onderzoekers ontwikkelen nieuwe tweestaps CO2-conversietechnologie
Kooldioxide transformeren - onderzoekers ontwikkelen nieuwe tweestaps CO2-conversietechnologie Begrijpen hoe een katalysator methaan omzet in etheen kan het affakkelen van aardgas voorkomen
Begrijpen hoe een katalysator methaan omzet in etheen kan het affakkelen van aardgas voorkomen Nieuw antischimmelmiddel van mierenboerderijen
Nieuw antischimmelmiddel van mierenboerderijen Waarom brandend metaal betekent reactie met zuurstof?
Waarom brandend metaal betekent reactie met zuurstof?  Hoe smakelijke kannibalenkrabben groot te brengen
Hoe smakelijke kannibalenkrabben groot te brengen
 Wat is actieve kool en waarom wordt het gebruikt in filters?
Wat is actieve kool en waarom wordt het gebruikt in filters?  NASA krijgt een nachtelijk beeld van ex-tropische cycloon Dineo
NASA krijgt een nachtelijk beeld van ex-tropische cycloon Dineo Wat is de structuur van water en de eigenschappen ervan in het menselijk lichaam?
Wat is de structuur van water en de eigenschappen ervan in het menselijk lichaam?  Bevingen in Lake Erie veroorzaakt door veranderende waterstanden? Studie vindt geen smoking gun, dringt aan op verder onderzoek
Bevingen in Lake Erie veroorzaakt door veranderende waterstanden? Studie vindt geen smoking gun, dringt aan op verder onderzoek Soorten ecosystemen in Texas
Soorten ecosystemen in Texas
Hoofdlijnen
- Wat is bacteriën het een producent?
- Beïnvloedt lichaamsritmes en interageert met de biologische klok?
- Wat hebben eukrayotische oproepen die prokaryotische cellen niet?
- Wat is een methode om kopieën van DNA te maken?
- Welk proces van celdeling produceert een exacte replica de cel?
- Wat is er in de landbouw?
- Hoeveel markers worden gebruikt om een DNA -profiel te maken?
- Wat is de wetenschappelijke naam voor Anaconda?
- Welk lichaamssysteem produceert hormonen om orgelactiviteit te reguleren?
- Bloemachtige nanostructuren in natriumbatterijen

- Nieuwe algoritmen waarvan is aangetoond dat ze het biofarmaceutische proces versnellen

- Het berekenen van de mollen die nodig zijn voor een chemische reactie:een praktische gids voor stoichiometrie

- Methoden voor machinaal leren bieden nieuwe inzichten in organisch-anorganische interfaces

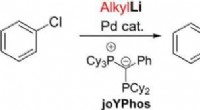
- Directe koppeling van arylhalogeniden en alkyllithiumverbindingen door palladiumkatalyse
 Ontdekking van hoe Taxol werkt zou kunnen leiden tot betere geneesmiddelen tegen kanker
Ontdekking van hoe Taxol werkt zou kunnen leiden tot betere geneesmiddelen tegen kanker  Wat is oscillatorie?
Wat is oscillatorie?  Waarom werden cellen niet waargenomen vóór de jaren 1600?
Waarom werden cellen niet waargenomen vóór de jaren 1600?  Wat zijn enkele voorbeelden van bewegingsenergie?
Wat zijn enkele voorbeelden van bewegingsenergie?  Wat was onze belangrijkste energiebron in 1950?
Wat was onze belangrijkste energiebron in 1950?  Lijst de takken van de biologie en de definitie ervan?
Lijst de takken van de biologie en de definitie ervan?  Bloomberg, Californisch team op klimaatsatellieten
Bloomberg, Californisch team op klimaatsatellieten 32.8 graden Celsius is gelijk aan hoeveel Fahrenheit?
32.8 graden Celsius is gelijk aan hoeveel Fahrenheit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

