
Wetenschap
Oplosbaarheid van ammoniak in water:waterstofbinding en polariteit uitgelegd
1. Waterstofbinding:
* Ammoniak heeft een eenzaam elektronenpaar op het stikstofatoom, waardoor het waterstofbruggen kan vormen met watermoleculen.
* Deze waterstofbruggen zijn sterke intermoleculaire krachten die aanzienlijk bijdragen aan de oplosbaarheid van ammoniak in water.
2. Polariteit:
* Het ammoniakmolecuul is polair vanwege het elektronegativiteitsverschil tussen stikstof- en waterstofatomen.
* Water is ook een polair molecuul.
* De aantrekkingskracht tussen het positieve uiteinde van het watermolecuul (waterstof) en het negatieve uiteinde van het ammoniakmolecuul (stikstof) verbetert de oplosbaarheid.
3. Vermogen om ammoniumionen te vormen:
* Wanneer ammoniak oplost in water, reageert het met watermoleculen om ammoniumionen (NH₄⁺) en hydroxide-ionen (OH⁻) te vormen:
NH₃(g) + H₂O(l) ⇌ NH₄⁺(aq) + OH⁻(aq)
* Deze reactie is een evenwichtsreactie en de vorming van ammoniumionen verbetert de oplosbaarheid van ammoniak in water verder.
4. Klein formaat:
* Ammoniakmoleculen zijn relatief klein, waardoor ze gemakkelijk kunnen interageren met watermoleculen en oplossen.
Algemeen:
De combinatie van waterstofbinding, polariteit, het vermogen om ammoniumionen te vormen en de kleine omvang zorgen ervoor dat ammoniak zeer oplosbaar is in water.
Opmerking: Hoewel ammoniak goed oplosbaar is in water, is het bij kamertemperatuur nog steeds een gas. De opgeloste ammoniakmoleculen vormen echter gemakkelijk ammoniumionen, die positief geladen zijn en daardoor in oplossing blijven.
 Welk organisch molecuul is het meest overvloedig?
Welk organisch molecuul is het meest overvloedig?  Hoe benzine werkt
Hoe benzine werkt  Welke elementen lijken het meest op zwavel?
Welke elementen lijken het meest op zwavel?  Wat is er gemaakt van alkali?
Wat is er gemaakt van alkali?  Hoe zouthloride af te voeren
Hoe zouthloride af te voeren
Zoutzuur, ook bekend als zoutzuur, de op water gebaseerde oplossing van waterstofchloride, is een zeer corrosief zuur. Het wordt gebruikt om batterijen en vuurwerk te maken, gelatine te maken en suiker te verwerken, maa
 Wat als er geen slangen waren?
Wat als er geen slangen waren?  De pirarucu:de gigantische gewaardeerde vis van de Amazone
De pirarucu:de gigantische gewaardeerde vis van de Amazone Waar vindt u geodes
Waar vindt u geodes Simulaties suggereren dat de zuurstofrijke atmosfeer van de aarde nog maar een miljard jaar meegaat
Simulaties suggereren dat de zuurstofrijke atmosfeer van de aarde nog maar een miljard jaar meegaat De belangrijkste op fosfor gebaseerde molecule voor het leven op aarde komt mogelijk uit de ruimte
De belangrijkste op fosfor gebaseerde molecule voor het leven op aarde komt mogelijk uit de ruimte
Hoofdlijnen
- Wanneer twee of meer populaties samenwonen, wordt het een genoemd?
- Waarom Australië de export van levende dieren verbiedt, kan een nettoverlies voor de welvaart betekenen
- Wat betekent inoculeren in de microbiologie?
- Structuur die het lichaam in 2 delen verdeelt?
- Wat is transcripton en vertaling die plaatsvindt tijdens eiwitsynthese?
- Bijenzoemen kunnen helpen bepalen hoe ze hun afnemende populatie kunnen redden
- Wat is het overvloedige eiwit in het menselijk lichaam?
- Hoe handelen planten snel om infecties te bestrijden?
- De functie van de visgonaden?
- Nieuwe synthetische biologietools ontgrendelen complexe plantengineering
- Vloeistof-vloeistof fasescheiding blijkt het proces van het omzetten van spidroïne-eiwitten in spinnenwebvezels te stimuleren
- Kokosolieverbindingen stoten insecten beter af dan DEET

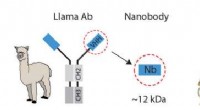
- Van lama afgeleide nanobodies als nieuw hulpmiddel bij het oplossen van kristalstructuur
- Veelgebruikte database van moleculaire vingerafdrukken geüpgraded

 H₃ Chemische formule:waarom deze niet bestaat - een wetenschappelijke verklaring
H₃ Chemische formule:waarom deze niet bestaat - een wetenschappelijke verklaring  Ze zijn er en ze zijn weg:ICARUS jaagt op een vierde neutrino
Ze zijn er en ze zijn weg:ICARUS jaagt op een vierde neutrino Mosselen en kokkels, schildwachten van de milieutoestand van de Nicaraguaanse kusten
Mosselen en kokkels, schildwachten van de milieutoestand van de Nicaraguaanse kusten Hoe wetenschap is nuttig voor de mensheid?
Hoe wetenschap is nuttig voor de mensheid?  Hoe microben de gezondheid van koraalriffen weerspiegelen
Hoe microben de gezondheid van koraalriffen weerspiegelen  Gegevens van Insight onthullen de grootte van de Mars-kern
Gegevens van Insight onthullen de grootte van de Mars-kern Waarom pikt een babyfoon video op van de spaceshuttle?
Waarom pikt een babyfoon video op van de spaceshuttle?  Facebook, Google en Amazon te groot? Waarom die vraag steeds weer opduikt
Facebook, Google en Amazon te groot? Waarom die vraag steeds weer opduikt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

