
Wetenschap
Niet-polaire covalente bindingen:gelijke verdeling van elektronen uitgelegd
Dit is waarom:
* Polaire covalente bindingen treden op wanneer de gedeelde elektronen ongelijk zijn gedeeld vanwege een verschil in elektronegativiteit tussen de atomen. Hierdoor ontstaat een gedeeltelijk positieve lading op het ene atoom en een gedeeltelijk negatieve lading op het andere.
* Niet-polaire covalente bindingen treedt op wanneer de gedeelde elektronen gelijk zijn gedeeld tussen atomen. Dit gebeurt wanneer de atomen vergelijkbare elektronegativiteiten hebben.
Elektronegativiteit is een maatstaf voor het vermogen van een atoom om elektronen in een binding aan te trekken. Wanneer twee atomen vergelijkbare elektronegativiteiten hebben, worden de elektronen gelijkelijk verdeeld, wat resulteert in een niet-polaire covalente binding.
Voorbeeld:
* Niet-polair: Een molecuul zuurstof (O2) heeft twee zuurstofatomen, die dezelfde elektronegativiteit hebben. De elektronen worden gelijkelijk gedeeld, waardoor een niet-polaire covalente binding ontstaat.
* Polair: Een molecuul water (H2O) heeft twee waterstofatomen en één zuurstofatoom. Zuurstof is elektronegatiever dan waterstof, dus de elektronen worden dichter bij het zuurstofatoom getrokken, waardoor een polaire covalente binding ontstaat.
Laat het me weten als je nog vragen hebt!
 Efficiënte en high-throughput techniek om de structuur van DNA te bestuderen
Efficiënte en high-throughput techniek om de structuur van DNA te bestuderen Hoe worden organische verbindingen geclassificeerd als ze met dezelfde moleculaire formule maar verschillende structurele formules hebben?
Hoe worden organische verbindingen geclassificeerd als ze met dezelfde moleculaire formule maar verschillende structurele formules hebben?  Efficiënte indiumoxidekatalysatoren ontworpen voor CO2-hydrogenering tot methanol
Efficiënte indiumoxidekatalysatoren ontworpen voor CO2-hydrogenering tot methanol Smakelijkere tomaten in de toekomst?
Smakelijkere tomaten in de toekomst?  Nieuwe alternatieven kunnen de vraag naar schaarse permanente magneten van zeldzame aardmetalen verminderen
Nieuwe alternatieven kunnen de vraag naar schaarse permanente magneten van zeldzame aardmetalen verminderen
 Wat is de wetenschappelijke wet van aantrekkingskracht?
Wat is de wetenschappelijke wet van aantrekkingskracht?  Hoe relevant wetenschap en technologie die relevant zijn voor je leven?
Hoe relevant wetenschap en technologie die relevant zijn voor je leven?  Studie onthult ongewoon hoge koolstofvoorraden en boomdiversiteit in het Darien-woud in Panama
Studie onthult ongewoon hoge koolstofvoorraden en boomdiversiteit in het Darien-woud in Panama How to Tell a Fawns Age
How to Tell a Fawns Age Zuid-Afrika moet opfrissen hoe het bijproducten van mijnbouw beheert
Zuid-Afrika moet opfrissen hoe het bijproducten van mijnbouw beheert
Hoofdlijnen
- Wat is de functie van avioli?
- Zijn lichaamsvloeistoffen isotone voor cellen?
- Welk proces gebruiken heterozygote organismen om energie vrij te geven?
- Ezels hebben meer bescherming nodig tegen de winter dan paarden
- Bevatten alle celorganellen een crista en matrix?
- Hoe bacteriën informatie opslaan om virussen te doden (maar niet zichzelf)
- Genetisch manipulatiemechanisme gevisualiseerd
- Uitkomsten van ziekten verschillen per nieuwe gastheersoort in experimenten met virusspillover
- Hoe evolueerden zenuwstelsels, met hun ongelooflijke complexiteit, tussen verschillende soorten?
- Hoe acrylplastic (PMMA) te vervaardigen:een gedetailleerde procesgids

- Mysterieuze cellulaire druppeltjes komen in beeld
- Wetenschappers creëren aanpasbare, stofachtige stroombron voor draagbare elektronica

- Constructie van op koolstof gebaseerde celachtige bollen voor robuuste kaliumanode
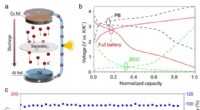
- Wetenschappers stemmen het systeem af om syngas te maken uit CO2
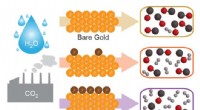
 Experimenten tonen aan dat de gegevens over het vroege leven volledig 'vals-positieven' kunnen zijn
Experimenten tonen aan dat de gegevens over het vroege leven volledig 'vals-positieven' kunnen zijn  Welk type rots wordt snel gevormd als gevolg van lava -koeling?
Welk type rots wordt snel gevormd als gevolg van lava -koeling?  Krachtige aardbeving schudt Zuid-Mexico, minstens 5 doden
Krachtige aardbeving schudt Zuid-Mexico, minstens 5 doden Chemici zien een vluchtige overgangstoestand van een reactie
Chemici zien een vluchtige overgangstoestand van een reactie Onderzoek onderzoekt waarom 'familie'-CEO's anders denken
Onderzoek onderzoekt waarom 'familie'-CEO's anders denken  Grafeen werkt samen met tweedimensionale kristallen voor snellere datacommunicatie
Grafeen werkt samen met tweedimensionale kristallen voor snellere datacommunicatie Er is hoop te midden van angst voor het milieu, zegt een geleerde van ecotheologie
Er is hoop te midden van angst voor het milieu, zegt een geleerde van ecotheologie AI heeft de kracht om de kredietverlening radicaal te veranderen, maar ten koste van mensen met lagere kredietscores
AI heeft de kracht om de kredietverlening radicaal te veranderen, maar ten koste van mensen met lagere kredietscores
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

