
Wetenschap
Koolstofobligaties:typen, eigenschappen en voorbeelden
1. Enkele obligaties: Koolstof deelt een elektron met een ander atoom en vormt zo een enkele binding. Dit is het meest voorkomende type bindingskoolstofvormen, weergegeven door een enkele lijn in structuurformules (bijv. C-H, C-C).
2. Dubbele obligaties: Koolstof deelt twee elektronen met een ander atoom en vormt zo een dubbele binding. Dit wordt weergegeven door twee lijnen in structuurformules (bijvoorbeeld C=C, C=O).
3. Drievoudige obligaties: Koolstof deelt drie elektronen met een ander atoom en vormt zo een drievoudige binding. Dit wordt weergegeven door drie lijnen in structuurformules (bijv. C≡C, C≡N).
4. Coördineer covalente obligaties: Hoewel het niet strikt genomen een afzonderlijk "type" binding is, kan koolstof ook deelnemen aan gecoördineerde covalente bindingen. In dit geval zijn beide elektronen in het gedeelde paar afkomstig van hetzelfde atoom (meestal een niet-metaal zoals zuurstof of stikstof).
Het is belangrijk op te merken dat het vermogen van koolstof om deze vier soorten bindingen te vormen een belangrijke reden is voor zijn veelzijdigheid en de enorme diversiteit aan organische verbindingen.
 Nieuwe manieren bedenken om onze planeet schoon te maken
Nieuwe manieren bedenken om onze planeet schoon te maken Waarom zuren opgeslagen in glazen containers in plaats van plastic?
Waarom zuren opgeslagen in glazen containers in plaats van plastic?  Welk soort gesteente zal het meest waarschijnlijk nieuwe verbindingen vormen wanneer het lucht heeft blootgelegd met zuren een gneis B kalksteen C graniet dschist?
Welk soort gesteente zal het meest waarschijnlijk nieuwe verbindingen vormen wanneer het lucht heeft blootgelegd met zuren een gneis B kalksteen C graniet dschist?  Hydrolysereacties:water toevoegen, niet verliezen | Chemie uitgelegd
Hydrolysereacties:water toevoegen, niet verliezen | Chemie uitgelegd  Wie heeft de chemische procesapparatuur geïntroduceerd?
Wie heeft de chemische procesapparatuur geïntroduceerd?
Hoofdlijnen
- De uiteindelijke cellen die voortvloeien uit meiose bij mannen of vrouwen worden genoemd?
- Wat is het principe van de celmembraanstructuur van een vloeibaar mozaïekmodel?
- Welke sierplanten presteren het beste voor bestuivers?
- Term voor organismen die de energie niet direct kunnen vangen en hun eigen voedsel maken?
- Waarom is osmose belangrijk voor het celmembraan?
- Is een dode organisme biotische of abiotische factor?
- Wat is de houder en beschermer van DNA?
- Gist brengt genetische variaties in de schijnwerpers die verband houden met resistentie tegen geneesmiddelen
- Is een enzymenfunctie afhankelijk van temperatuur en pH?
- Duurzame chemie op kwantumniveau

- Video:Kan er leven zijn zonder koolstof?

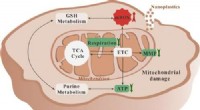
- Nanoplastics kunnen menselijke lever- en longcelprocessen verstoren in laboratoriumexperimenten
- AI- en NMR-spectroscopie bepalen in recordtijd de configuratie van atomen
- Nieuwe, door licht aangedreven katalysatoren kunnen helpen bij de productie

 Hoe de leidende crisis in Amerika aan te pakken en iedereen veilig drinkwater te bieden?
Hoe de leidende crisis in Amerika aan te pakken en iedereen veilig drinkwater te bieden? De deeltjesvolgkracht van het algoritme benutten
De deeltjesvolgkracht van het algoritme benutten Druppelverspreiding door mensen volgt niet altijd de luchtstroom
Druppelverspreiding door mensen volgt niet altijd de luchtstroom Term de beste voorwaarden voor een bestaan van een organismen?
Term de beste voorwaarden voor een bestaan van een organismen?  Wat zijn graniet en basalt?
Wat zijn graniet en basalt?  Amerikaanse jongeren weten niet veel over het jeugdrechtsysteem
Amerikaanse jongeren weten niet veel over het jeugdrechtsysteem Wat is de lijn door middel van een quasar?
Wat is de lijn door middel van een quasar?  Wat is versnelling van de zwaartekracht?
Wat is versnelling van de zwaartekracht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

