
Wetenschap
Waterstofbinding:de aantrekkingskracht tussen polaire moleculen begrijpen
Hier is een overzicht:
* Polaire covalente obligaties: Er vormen zich waterstofbruggen tussen moleculen die polaire covalente bindingen hebben. Bij deze bindingen worden elektronen ongelijk verdeeld tussen de atomen.
* Gedeeltelijke kosten: Het atoom met een hogere elektronegativiteit (trekt elektronen sterker aan) krijgt een gedeeltelijk negatieve lading (δ-), terwijl het andere atoom een gedeeltelijk positieve lading krijgt (δ+). In een watermolecuul (H₂O) is zuurstof bijvoorbeeld elektronegatiever dan waterstof, waardoor zuurstof een δ- en waterstof een δ+ krijgt.
* Waterstofbinding: Het gedeeltelijk positieve waterstofatoom (δ+) van het ene molecuul wordt aangetrokken door het gedeeltelijk negatieve atoom (δ-) van een ander molecuul. Deze aantrekkingskracht wordt een waterstofbrug genoemd.
Belangrijkste kenmerken van waterstofbinding:
* Sterker dan Van der Waals-krachten, maar zwakker dan ionische of covalente bindingen.
* Speelt een cruciale rol in veel biologische processen en chemische reacties.
* Verantwoordelijk voor het hoge kookpunt van water en de structuur van DNA.
Laat het me weten als je een van deze aspecten nader wilt onderzoeken!
 Doelstellingen van de viskwekerij
Doelstellingen van de viskwekerij Wat is het verschil tussen een biosfeer en gemeenschap?
Wat is het verschil tussen een biosfeer en gemeenschap?  Satellietbeelden stormsysteem dat Zuid-Californië treft
Satellietbeelden stormsysteem dat Zuid-Californië treft Stijgende kooldioxidegehaltes zullen mariene habitats en visgemeenschappen veranderen
Stijgende kooldioxidegehaltes zullen mariene habitats en visgemeenschappen veranderen Hoe klaproosbloemen die levendige kleuren krijgen die insecten lokken
Hoe klaproosbloemen die levendige kleuren krijgen die insecten lokken
Hoofdlijnen
- Hoe orale culturen zoveel informatie onthouden
- Wat is de algen die een symbiotische relatie hebben met rifbuilders?
- Wat is de variabele die door wetenschappers wordt bestuurd?
- Geef punten, advocaat Thst Biology is gekoppeld aan Physics Chemistry Mathsmatics Geography?
- Mariene microplastics:hoe de verspreiding van watermassa de transporttrajecten beïnvloedt
- Wat is de functie van hormonen in cel?
- Wat is een verklaring over de bevolkingsleden die lang genoeg leven om consistent te reproduceren met de theorie -evolutie door de natuurwetenschap?
- Wat worden granulocyten?
- Leg de rol van X- en Y -chromosomen uit bij het bepalen van het geslacht?
- Wetenschappers gaan ver in studie naar elektronenoverdracht
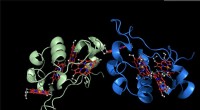
- Kijken naar atomen die bewegen in hybride perovskietkristallen onthult aanwijzingen voor het verbeteren van zonnecellen

- Geneesmiddelgeïnduceerde celmembraancomplexen induceren de dood van kankercellen

- Zelfassemblerende polymeren op siliconenbasis
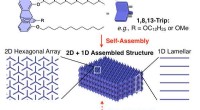
- Op het netvlies geïnspireerde fotonische synapsen op basis van koolstofnitride voor selectieve detectie van UV-licht
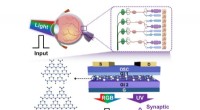
 Is de fysische of chemische eigenschap van wijn?
Is de fysische of chemische eigenschap van wijn?  Stikstof uit biologische vaste stoffen kan stedelijke bodems en plantengroei helpen
Stikstof uit biologische vaste stoffen kan stedelijke bodems en plantengroei helpen NASA legt de laatste buiging van Kai-Taks in tropische depressie vast
NASA legt de laatste buiging van Kai-Taks in tropische depressie vast Welk kenmerk gebruiken wetenschappers om sponzen te classificeren?
Welk kenmerk gebruiken wetenschappers om sponzen te classificeren?  SPAD VII &SPAD XIII
SPAD VII &SPAD XIII  Welke van de landen hebben wetenschappers onlangs muizen opgericht door twee genetische moeders en geen vaders te gebruiken?
Welke van de landen hebben wetenschappers onlangs muizen opgericht door twee genetische moeders en geen vaders te gebruiken?  Waarom duurt het 164 Earth Years voordat Neptunus om de zon draait en kost het slechts 0,24 jaar kwik?
Waarom duurt het 164 Earth Years voordat Neptunus om de zon draait en kost het slechts 0,24 jaar kwik?  Wetenschappers gebruiken nieuwe methode om veelbelovend batterijmateriaal te maken
Wetenschappers gebruiken nieuwe methode om veelbelovend batterijmateriaal te maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

