
Wetenschap
Kristalroosters in ionische verbindingen begrijpen:structuur en binding
1. Ionen: Ionische verbindingen bestaan uit positief geladen ionen (kationen) en negatief geladen ionen (anionen).
2. Elektrostatische aantrekkingskracht: De tegengestelde ladingen van deze ionen trekken elkaar aan, waardoor een sterke elektrostatische kracht ontstaat die ze bij elkaar houdt.
3. Herhalend patroon: Deze aantrekkingskracht dwingt de ionen om zichzelf in een specifiek, herhalend patroon te ordenen, waardoor een roosterstructuur ontstaat. Dit patroon strekt zich uit in alle richtingen en creëert een enorm, onderling verbonden netwerk van ionen.
4. Eenheidscel: De kleinste herhalende eenheid van het rooster wordt de eenheidscel genoemd. Het is als een bouwsteen die, wanneer hij in alle richtingen wordt herhaald, de hele kristalstructuur creëert.
5. Roosterpunten: De locaties van de ionen binnen de eenheidscel worden roosterpunten genoemd. Deze punten zijn niet zomaar willekeurig, maar precies gedefinieerd binnen de driedimensionale ruimte van het kristal.
Waarom is het kristalrooster belangrijk?
* Stabiliteit: De roosterstructuur is cruciaal voor de stabiliteit van ionische verbindingen. De sterke elektrostatische aantrekkingskracht tussen de ionen is de belangrijkste kracht die de verbinding bij elkaar houdt.
* Vorm en eigenschappen: De rangschikking van ionen in het rooster bepaalt de algehele vorm en fysieke eigenschappen van het kristal, zoals het smeltpunt, de hardheid en de geleidbaarheid.
* Reactiviteit: De roosterstructuur kan ook beïnvloeden hoe gemakkelijk een ionische verbinding reageert met andere stoffen.
Voorbeeld:
Natriumchloride (NaCl), of keukenzout, is een bekend voorbeeld van een ionische verbinding. Het kristalrooster is een kubieke structuur met het gezicht in het midden. In deze structuur wisselen natriumionen (Na+) en chloride-ionen (Cl-) elkaar af in een driedimensionale opstelling, waardoor een stabiel, zich herhalend patroon ontstaat.
Het begrijpen van kristalroosters is van fundamenteel belang voor het begrijpen van het gedrag en de eigenschappen van ionische verbindingen.
 Is SO3 een niet -metaal of metaal?
Is SO3 een niet -metaal of metaal?  Zal het verhogen van de hoeveelheid beperkende reactant in een reactie het percentage opbrengst verhogen?
Zal het verhogen van de hoeveelheid beperkende reactant in een reactie het percentage opbrengst verhogen?  Nieuwe aanpak bepaalt optimale materiaalontwerpen met minimale gegevens
Nieuwe aanpak bepaalt optimale materiaalontwerpen met minimale gegevens Het effect van additieven op de kristallisatie van calciumcarbonaat
Het effect van additieven op de kristallisatie van calciumcarbonaat  Wetenschappers ontwikkelen sterke maar herbruikbare lijm uit slimme materialen
Wetenschappers ontwikkelen sterke maar herbruikbare lijm uit slimme materialen
 Radarsatellieten kunnen beter beschermen tegen bosbranden en overstromingen
Radarsatellieten kunnen beter beschermen tegen bosbranden en overstromingen Modelontwikkeling is cruciaal om klimaatverandering te begrijpen
Modelontwikkeling is cruciaal om klimaatverandering te begrijpen Klimaatwetenschappers zijn geloofwaardiger als ze praktiseren wat ze prediken
Klimaatwetenschappers zijn geloofwaardiger als ze praktiseren wat ze prediken  Schok, angst en verdriet houden de Australische bosbrandvluchtelingen in de greep
Schok, angst en verdriet houden de Australische bosbrandvluchtelingen in de greep Bosverlies Zuidoost-Azië groter dan verwacht, met negatieve klimaatimplicaties
Bosverlies Zuidoost-Azië groter dan verwacht, met negatieve klimaatimplicaties
Hoofdlijnen
- Hoe neuronale herkenning van zangvogelgeluiden zich in de loop van de tijd ontvouwt
- Wat is de cel van een organisme waarvan een virus afhankelijk is?
- Wat doet een plantcel?
- Nieuw onderzoek met video laat zien hoe vrouwelijke kikkers zich verdedigen tegen ongewenste paring
- Welke verpakkingen en draagt eiwitten voor cellen?
- Waarom classificeer je levende wezens als biologen?
- Het Human Genome Project kan genetische ingenieurs helpen bij het produceren van menselijke eiwitten omdat?
- Waar worden mesenchymale stamcellen voor gebruikt?
- Pas op voor de huisdieren bij het hanteren van de Halloween-snoepvangst
- Onderzoekers ontdekken de oorsprong van bijna-ultraviolette en zichtbare absorptiekenmerken van Ti:saffierlaserkristallen
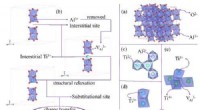
- Onderzoekers vinden potentiële nieuwe bron van zeldzame aardelementen

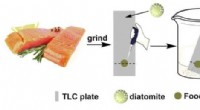
- Gefossiliseerde algen zijn veelbelovend voor verbeterde voedselveiligheidstesten
- Stapsgewijze handleiding voor het tekenen van nauwkeurige atoommodellen
- Eerste snapshots van ingesloten CO2-moleculen werpen nieuw licht op koolstofafvang

 Achterstoelen van auto's hebben betere veiligheidsuitrusting nodig, studie zegt:
Achterstoelen van auto's hebben betere veiligheidsuitrusting nodig, studie zegt: Methanolbiotransformatie maakt efficiënte productie van vetzuren uit gist mogelijk
Methanolbiotransformatie maakt efficiënte productie van vetzuren uit gist mogelijk Wanneer vormen invasieve soorten een bedreiging?
Wanneer vormen invasieve soorten een bedreiging?  Gemanipuleerde microben kunnen biologisch afbreekbare kunststoffen produceren tegen lagere kosten en milieu-impact dan plantaardige kunststoffen
Gemanipuleerde microben kunnen biologisch afbreekbare kunststoffen produceren tegen lagere kosten en milieu-impact dan plantaardige kunststoffen Bayesiaanse jachtramp:hoe gespecialiseerde zoek- en reddingsteams onder water werken
Bayesiaanse jachtramp:hoe gespecialiseerde zoek- en reddingsteams onder water werken  NASA ziet tropische cycloon Carlos ten zuiden van het eiland La Réunion
NASA ziet tropische cycloon Carlos ten zuiden van het eiland La Réunion Wat is de basiseenheid van biosfeer?
Wat is de basiseenheid van biosfeer?  Hoe wordt energie overgedragen?
Hoe wordt energie overgedragen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

