
Wetenschap
Chloor versus argon:reactiviteit en elektronenconfiguratie begrijpen
Hier is een overzicht:
Chloor (Cl)
* Elektronenconfiguratie: [Ne] 3s² 3p⁵
* Valentie-elektronen: 7 (in de buitenste 3p-schaal)
Chloor is zeer reactief omdat het één elektron tekort heeft van het hebben van een volledige buitenschil (wat een stabiele, energiezuinige toestand is). Om deze stabiele toestand te bereiken, krijgt chloor gemakkelijk één elektron door een chemische reactie. Dit maakt het een sterk oxidatiemiddel, wat betekent dat het gemakkelijk elektronen van andere atomen accepteert.
Argon (Ar)
* Elektronenconfiguratie: [Ne] 3s² 3p⁶
* Valentie-elektronen: 8 (in de buitenste 3p-schaal)
Argon heeft een volledige buitenlaag van elektronen, waardoor het ongelooflijk stabiel is. Het hoeft geen elektronen te winnen of te verliezen om een stabiele configuratie te bereiken. Dit maakt het inert , wat betekent dat het zelden deelneemt aan chemische reacties.
Samengevat:
* Chloor reactiviteit komt voort uit de wens om één elektron te verkrijgen om een stabiele, volledige buitenschil te bereiken.
* Argon traagheid komt voort uit het al hebben van een stabiele, volledige buitenschaal.
 Wat is de figuur die het aantal identieke moleculen in een formule geeft?
Wat is de figuur die het aantal identieke moleculen in een formule geeft?  Plantenonderzoekers onderzoeken broodaroma:moderne en oude tarwesoorten smaken even goed
Plantenonderzoekers onderzoeken broodaroma:moderne en oude tarwesoorten smaken even goed Zwavelzuur- en nikkelreactie:oxidatie begrijpen
Zwavelzuur- en nikkelreactie:oxidatie begrijpen  Hoe schrijf je de halve levensduur van uranium 238 als standaardnummer?
Hoe schrijf je de halve levensduur van uranium 238 als standaardnummer?  Acetal wordt gebruikt bij de productie van welke montage?
Acetal wordt gebruikt bij de productie van welke montage?
 Wat is de specifieke omgeving waaraan een soort zich heeft aangepast?
Wat is de specifieke omgeving waaraan een soort zich heeft aangepast?  Wat is de grootste soort dieren in Colorado?
Wat is de grootste soort dieren in Colorado?  Onbekende wateren:wetenschappers gaan de diepten van de Indische Oceaan verkennen
Onbekende wateren:wetenschappers gaan de diepten van de Indische Oceaan verkennen Overstromingen, stormvloed kan net zo verwoestend zijn als de wind van een orkaan
Overstromingen, stormvloed kan net zo verwoestend zijn als de wind van een orkaan Noord-Amerikaanse bossen met een koud klimaat nemen al minder koolstof op, studie toont
Noord-Amerikaanse bossen met een koud klimaat nemen al minder koolstof op, studie toont
Hoofdlijnen
- Wie stelde voor dat organismen tijdens hun leven eigenschappen hebben verworven of verloren door selectief gebruik niet te gebruiken van organen?
- Wat is een wetenschappelijk idee?
- Welk hulpmiddel zou een levenswetenschapper gebruiken om driedimensionaal beeld van microscopisch organisme te krijgen?
- Waar vindt meiose plaats in bryophytes?
- Waar vindt eiwitsynthisis plaats?
- Californië wordt geconfronteerd met een recorduitbraak van paddestoelvergiftiging:35 ziekenhuisopnames, 3 dodelijke slachtoffers door Death Caps
- Wat is de stroom van ideogenese?
- Verborgen biosfeer ontdekt onder de droogste hete woestijn ter wereld
- Menselijke sterke en zwakke punten:een biologisch perspectief
- SpaceMat:Graphenes antwoord op de lancering van rubber voor recycling van banden op de markt

- Kwantificeren van veranderingen in oppervlaktechemie van houtachtige planten tijdens microbiële fermentatie
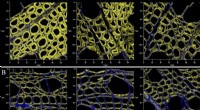
- De onderbuik van kreeften is net zo sterk als industrieel rubber

- Nieuwe glasfamilie goed voor lenzen

- Methode om de atomaire structuur van natrium-ionbatterijen te voorspellen

 Gepolariseerde microscopietechniek toont nieuwe details van hoe eiwitten zijn gerangschikt
Gepolariseerde microscopietechniek toont nieuwe details van hoe eiwitten zijn gerangschikt  Hoe kan een exacte 0,1N-oplossing NaOH worden bereid?
Hoe kan een exacte 0,1N-oplossing NaOH worden bereid?  Welke hoeveelheid wordt gemeten door Newton?
Welke hoeveelheid wordt gemeten door Newton?  Welke gespecialiseerde weefsels hebben vasculaire planten die andere niet?
Welke gespecialiseerde weefsels hebben vasculaire planten die andere niet?  Beschrijf de vereisten voor een materiaal dat moet worden geclassificeerd als sedimentair gesteente?
Beschrijf de vereisten voor een materiaal dat moet worden geclassificeerd als sedimentair gesteente?  Russische raket lanceert 34 nieuwe Britse satellieten
Russische raket lanceert 34 nieuwe Britse satellieten Veren, cognitie en mondiaal consumentisme in het koloniale Amazonegebied
Veren, cognitie en mondiaal consumentisme in het koloniale Amazonegebied  Nieuwe inzichten in hoe gels ontstaan
Nieuwe inzichten in hoe gels ontstaan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

