Wetenschap
Behoudswetten in de H₂ + Cl₂ → 2HCl-reactie
* Massa: De totale massa van de reactanten (H₂ en Cl₂) is gelijk aan de totale massa van het product (HCl). Dit komt door de wet van behoud van massa, die stelt dat massa niet kan worden gecreëerd of vernietigd door een chemische reactie.
* Atomen: Het aantal waterstof- en chlooratomen aan de reactantzijde (2 waterstofatomen en 2 chlooratomen) is gelijk aan het aantal waterstof- en chlooratomen aan de productzijde (2 waterstofatomen en 2 chlooratomen). Dit komt door de wet van behoud van atomen, die stelt dat atomen bij een chemische reactie niet ontstaan of vernietigd worden.
* Energie: Terwijl bij de reactie energie vrijkomt (deze is exotherm), blijft de totale energie van het systeem constant. Dit komt door de wet van behoud van energie, die stelt dat energie niet kan worden gecreëerd of vernietigd, maar alleen kan worden omgezet van de ene vorm in de andere.
Het is belangrijk op te merken dat hoewel de algehele reactie deze hoeveelheden behoudt, de specifieke vormen van energie en de rangschikking van atomen kunnen veranderen.
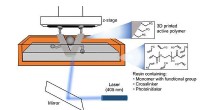
 Door te sporten werken hydrogels meer als spieren
Door te sporten werken hydrogels meer als spieren Wat hebben substantie en mengsel gemeen?
Wat hebben substantie en mengsel gemeen?  Wat is het aantal protonen -elektronen en neutronen in één atoomchloor 37?
Wat is het aantal protonen -elektronen en neutronen in één atoomchloor 37?  Welke ring van fenylbenzoaat zou gemakkelijker nitratie ondergaan?
Welke ring van fenylbenzoaat zou gemakkelijker nitratie ondergaan?  Wat zijn de intermoleculaire aantrekkingskrachten tussen HCl-moleculen?
Wat zijn de intermoleculaire aantrekkingskrachten tussen HCl-moleculen?
Hoofdlijnen
- Welke drie dingen stelt de oorspronkelijke celtheorie voor?
- USDA verstrooiende rabiësvaccins voor dieren in het wild in 13 staten
- Welke eigenschap kan een menselijk nageslacht erven?
- Voelen planten pijn?
- Stelt de celtheorie dat alle cellen voortkomen uit andere cellen?
- Vat 3 wetten samen en hoe zij veel erfenispatronen bepalen?
- Een organisatie wiens allelen voor eigenschappen identiek zijn?
- Wat betekent een deuterostomes?
- Wat is de definitie van diplo -celregeling in bacteriën?
 Hoe breuken af te trekken
Hoe breuken af te trekken  Is Afrika de bakermat van de mensheid?
Is Afrika de bakermat van de mensheid?  Marsoppervlak hardde snel uit, levenskansen vergroten:studeren
Marsoppervlak hardde snel uit, levenskansen vergroten:studeren Dat beschrijft een treinen versnelling als deze van snelheid van 25 ms in 10 ms in 240s verandert?
Dat beschrijft een treinen versnelling als deze van snelheid van 25 ms in 10 ms in 240s verandert?  Nieuwe beeldvormingsbenadering visualiseert hoe het uitoefenen van kracht op eiwitten complexe formaties verandert
Nieuwe beeldvormingsbenadering visualiseert hoe het uitoefenen van kracht op eiwitten complexe formaties verandert  Is aardgas lichter of zwaarder dan lucht?
Is aardgas lichter of zwaarder dan lucht?  Onderzoekers zeggen dat de eerste atomaire blik op ferro-elektrische nanokristallen wijst op terabytes/inch-opslag
Onderzoekers zeggen dat de eerste atomaire blik op ferro-elektrische nanokristallen wijst op terabytes/inch-opslag Wat zijn lage energiegolven gevonden in het elektromagnetisch spectrum genoemd?
Wat zijn lage energiegolven gevonden in het elektromagnetisch spectrum genoemd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com