
Wetenschap
Bereken de molaire massa van azijnzuur via kookpuntverhoging
Het concept begrijpen
De verhogingskookpuntmethode is gebaseerd op het principe dat het toevoegen van een niet-vluchtige opgeloste stof aan een oplosmiddel het kookpunt van het oplosmiddel verhoogt. De omvang van deze verhoging is recht evenredig met de molaliteit van de oplossing.
De vergelijking
De vergelijking die de kookpuntverhoging (ΔTb) relateert aan de molaliteit (m) van de oplossing is:
ΔTb =Kb * m
Waar:
* ΔTb =Verandering in kookpunt (in °C)
* Kb =Ebullioscopische constante van het oplosmiddel (in °C kg/mol)
* m =Molaliteit van de oplossing (in mol/kg)
Stappen om de molaire massa te bepalen
1. Bereid de oplossing voor:
* Los een bekend gewicht (w) azijnzuur op in een bekend gewicht (W) van een geschikt oplosmiddel (bijvoorbeeld water).
2. Meet de kookpunthoogte:
* Bepaal het kookpunt van het zuivere oplosmiddel (Tb(solvent)).
* Meet het kookpunt van de oplossing (Tb(oplossing)).
* Bereken de kookpuntverhoging:ΔTb =Tb(oplossing) - Tb(oplosmiddel)
3. Bepaal de molaliteit:
* Je kent de kookpuntverhoging (ΔTb) en de ebullioscopische constante (Kb) voor het oplosmiddel.
* Gebruik de vergelijking ΔTb =Kb * m om de molaliteit (m) op te lossen.
4. Bereken de molmassa:
* Molaliteit (m) =mol opgeloste stof / kg oplosmiddel
* Je kent het gewicht van de opgeloste stof (w) en het gewicht van het oplosmiddel (W).
* Herschik de molaliteitsvergelijking om het aantal mol opgeloste stof op te lossen:
mol opgeloste stof =m * W (in kg)
* Molaire massa (M) =gewicht opgeloste stof (w) / mol opgeloste stof
Voorbeeld
Stel dat u 1,00 g azijnzuur oplost in 100 g water. De ebullioscopische constante voor water is 0,512 °C kg/mol. Je meet een kookpuntverhoging van 0,15 °C.
1. Kookpunthoogte: ΔTb =0,15 °C
2. Molaliteit:
* 0,15 °C =0,512 °C kg/mol * m
* m =0,15 °C / 0,512 °C kg/mol =0,293 mol/kg
3. Molen azijnzuur:
* mol azijnzuur =0,293 mol/kg * 0,100 kg =0,0293 mol
4. Molaarmassa:
* Molaire massa =1,00 g / 0,0293 mol =34,2 g/mol
Belangrijke opmerkingen:
* Oplosmiddelkeuze: Het oplosmiddel moet niet-vluchtig zijn en een bekende ebullioscopische constante hebben.
* Nauwkeurigheid: De nauwkeurigheid van deze methode is afhankelijk van nauwkeurige metingen van temperatuur en gewicht.
* Ideale omstandigheden: Deze methode gaat uit van het ideale gedrag van de oplossing.
De werkelijke molaire massa van azijnzuur is 60,05 g/mol. Het resultaat van dit experiment is aanzienlijk lager vanwege de beperkingen van de methode en mogelijke experimentele fouten.
 Een molecuul alkeen heeft de chemische formule C3H4. Hoeveel dubbele koolstof-koolstofbindingen zijn er aanwezig in het molecuul?
Een molecuul alkeen heeft de chemische formule C3H4. Hoeveel dubbele koolstof-koolstofbindingen zijn er aanwezig in het molecuul?  Welke stof bevat koolzuur?
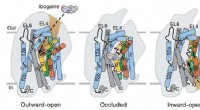
Welke stof bevat koolzuur?  Een beter begrip van nanomachines van de natuur kan helpen bij het ontwerpen van toekomstige medicijnen
Een beter begrip van nanomachines van de natuur kan helpen bij het ontwerpen van toekomstige medicijnen Wat is de naam gemeenschappelijke zuren aanwezig in oliën en vetten?
Wat is de naam gemeenschappelijke zuren aanwezig in oliën en vetten?  Een lithiumatoom dat een elektron heeft verloren, komt in de buurt van een chloor gekregen elektron. Wat gebeurt er?
Een lithiumatoom dat een elektron heeft verloren, komt in de buurt van een chloor gekregen elektron. Wat gebeurt er?
Hoofdlijnen
- Welke dingen gebruiken een membraangebonden systeem dat cytochromen bevat om ATP te produceren?
- Tagging-project werpt licht op de ongrijpbare witte haai
- Meer dan een tiende van 's werelds terrestrische genetische diversiteit is mogelijk al verloren gegaan, zegt onderzoek
- Wat betekent homeotase?
- Waarom zijn enzymen belangrijk in een cel?
- Wat betekent genetisch identiek?
- Welke van deze structuren is uniek voor plantencellen?
- Hoe identificeren en categoriseren wetenschappers nieuwe organismen?
- Wat zijn enkele nuttige Mirco -organismen?
- Video:Hoe melk kaas wordt

- Bacterieel eiwit bootst DNA na om de afweer van cellen te saboteren

- Onderzoekers ontwikkelen materialen die een revolutie teweeg kunnen brengen in de manier waarop licht wordt gebruikt voor zonne-energie

- Nieuw additief helpt onderzoekers om CO2 selectiever om te zetten in multicarbon-brandstoffen

- Verslaving behandelen:Cryo-EM-technologie maakt het onmogelijke mogelijk
 Deze felblauwe kleurstof is te vinden in stof. Kan het ook batterijen van stroom voorzien?
Deze felblauwe kleurstof is te vinden in stof. Kan het ook batterijen van stroom voorzien? Welke van de volgende kan gebeuren met zonne -energie nadat het de atmosfeer binnengaat?
Welke van de volgende kan gebeuren met zonne -energie nadat het de atmosfeer binnengaat?  Hoe plantenhormonen de wortelgroei controleren
Hoe plantenhormonen de wortelgroei controleren  Schrijf voor water een zin over de fysieke veranderingen?
Schrijf voor water een zin over de fysieke veranderingen?  Conglomeraten behoren tot een groep sedimentaire rotsen die worden genoemd?
Conglomeraten behoren tot een groep sedimentaire rotsen die worden genoemd?  Het werk dat nodig is om een object op een wrijvingsloos oppervlak van snelheid V 2V te versnellen?
Het werk dat nodig is om een object op een wrijvingsloos oppervlak van snelheid V 2V te versnellen?  Wat is de evenwichtige vergelijking van ijzeroxide en zoutzuur uit reactiechloridewater?
Wat is de evenwichtige vergelijking van ijzeroxide en zoutzuur uit reactiechloridewater?  Wat zijn feiten over de wassende maansikkel?
Wat zijn feiten over de wassende maansikkel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

