
Wetenschap
Natrium, fluor en neon:chemische reactiviteit begrijpen
1. Elektronenconfiguratie
* Natrium (Na): Heeft één elektron in zijn buitenste schil (valentieschil). Het verliest dit elektron gemakkelijk om een stabiele octetconfiguratie te bereiken, zoals het edelgas-neon. Dit maakt natrium zeer reactief, vooral met niet-metalen die elektronen willen winnen.
* Fluor (F): Heeft zeven elektronen in zijn valentieschil. Het verkrijgt gemakkelijk één elektron om een stabiele octetconfiguratie te bereiken, zoals het edelgas-neon. Dit maakt fluor zeer reactief, vooral met metalen die elektronen willen verliezen.
* Neon (Ne): Heeft een volledig octet aan elektronen in zijn valentieschil. Dit betekent dat het al stabiel is en geen elektronen hoeft te winnen of te verliezen, waardoor het niet-reactief is.
2. Elektronegativiteit
* Fluor: Is het meest elektronegatieve element, wat betekent dat het een sterke aantrekkingskracht heeft op elektronen. Dit maakt het tot een krachtig oxidatiemiddel dat gemakkelijk elektronen uit andere atomen trekt.
* Natrium: Heeft een lage elektronegativiteit, wat betekent dat het gemakkelijk elektronen verliest. Dit maakt het tot een krachtig reductiemiddel, dat gemakkelijk elektronen afstaat aan andere atomen.
* Neon: Heeft een zeer lage elektronegativiteit vanwege de volledige buitenschil. Het trekt noch gemakkelijk elektronen aan, noch verliest het, waardoor het niet-reactief is.
3. Ionisatie-energie en elektronenaffiniteit
* Natrium: Heeft een lage ionisatie-energie, wat betekent dat er relatief weinig energie nodig is om het buitenste elektron te verwijderen. Hierdoor kan natrium gemakkelijk positieve ionen vormen.
* Fluor: Heeft een hoge elektronenaffiniteit, wat betekent dat er een grote hoeveelheid energie vrijkomt wanneer het een elektron opneemt. Hierdoor kan fluor gemakkelijk negatieve ionen vormen.
* Neon: Heeft een zeer hoge ionisatie-energie en lage elektronenaffiniteit. Dit betekent dat het erg moeilijk is om een elektron uit neon te verwijderen of er een te verwerven.
Samengevat:
* Natrium en fluor zijn zeer reactief vanwege hun neiging om elektronen te winnen of te verliezen om stabiele octetten te bereiken.
* Neon is inert omdat het al een stabiel octet heeft, wat betekent dat het geen drijvende kracht heeft om deel te nemen aan chemische reacties.
Dit is een vereenvoudigde uitleg, maar benadrukt de belangrijkste factoren die de reactiviteit bepalen in de context van natrium, fluor en neon.
 Recycling van plastic:vinylpolymeer afgebroken tot aspirinecomponenten
Recycling van plastic:vinylpolymeer afgebroken tot aspirinecomponenten Nieuwe klasse katalysatoren voor energieconversie
Nieuwe klasse katalysatoren voor energieconversie Wat is de moleculaire vergelijking voor lood II -acetaat die reageert met kaliumchromaat?
Wat is de moleculaire vergelijking voor lood II -acetaat die reageert met kaliumchromaat?  Welke stoffen bevatten polyatomaire ionen?
Welke stoffen bevatten polyatomaire ionen?  Nieuwe hogesnelheidstest laat zien hoe antibiotica samen bacteriën doden
Nieuwe hogesnelheidstest laat zien hoe antibiotica samen bacteriën doden
Hoofdlijnen
- Hoeveel cellen worden er gevormd tijdens mitose en ze identiek?
- Wat is waar aan alle wetenschappelijke modellen?
- Hoe gebruiken cellen een hoog caloriemolecuul zoals glucose?
- Welk type RNA bevat codons?
- Parasiteonderzoekers smelten eiwitten om hun rol bij infectie te begrijpen
- Hoe beïnvloeden milieuchemicaliën gieren?
- Met software kunnen onderzoekers kleine ronde voorwerpen uit DNA maken. Dit is waarom dat cool is
- Wat is een boom met fruit die eruit ziet als ronde hersenen?
- Kevers vertrouwen op unieke achterzakken om bacteriële symbionten veilig te houden tijdens metamorfose
- Ingenieurs ontwikkelen botachtig metaalschuim dat bij kamertemperatuur kan worden genezen

- Onderzoekers volgen eiwitbinding, bouwen synthetische eiwitten om genexpressie te bestuderen

- Ruiken in kleine huisjes:hoe ciliaire elektrische stromen de reuk betrouwbaar houden

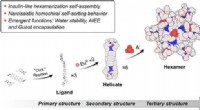
- Hexamere lanthanide-organische capsules met tertiaire structuur, opkomende functies
- De stof van wandeluitrusting heeft een verkoelend effect dat uw volgende smartwatch comfortabeler kan maken

 Hoe zijn dieren en anders?
Hoe zijn dieren en anders?  Anatomie:oorsprong en de wetenschap van de biologische structuur
Anatomie:oorsprong en de wetenschap van de biologische structuur  Ultradun, gasdichte coatings voor PET-flessen
Ultradun, gasdichte coatings voor PET-flessen Math wiskunde leuk maken voor kinderen
Math wiskunde leuk maken voor kinderen Wat is het aandeel lichtenergie?
Wat is het aandeel lichtenergie?  Hoe ruikt een wetenschappelijk lab?
Hoe ruikt een wetenschappelijk lab?  Hoe je 'spookvijvers' uit de dood kunt wekken
Hoe je 'spookvijvers' uit de dood kunt wekken  Hoe kan een chemische reactie de tas laten opblazen?
Hoe kan een chemische reactie de tas laten opblazen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

