
Wetenschap
Kaliumchloride begrijpen:waarom het ionische bindingen vormt
* Elektronegativiteit: Elektronegativiteit is een maatstaf voor het vermogen van een atoom om elektronen naar zich toe te trekken in een chemische binding.
* Kalium (K): Kalium is een metaal met een lage elektronegativiteit. Het verliest gemakkelijk zijn buitenste elektron om een stabiele elektronenconfiguratie te bereiken.
* Chloor (Cl): Chloor is een niet-metaal met een hoge elektronegativiteit. Het verkrijgt gemakkelijk een elektron om een stabiele elektronenconfiguratie te bereiken.
De vorming van de ionische binding:
1. Wanneer kalium en chloor reageren, verliest kalium zijn ene valentie-elektron en wordt het een positief geladen ion (K+).
2. Chloor verkrijgt dat elektron en wordt een negatief geladen ion (Cl-).
3. De tegengesteld geladen ionen trekken elkaar elektrostatisch aan en vormen een ionische binding.
Kenmerken van ionverbindingen:
* Sterke elektrostatische krachten: De sterke aantrekkingskracht tussen de tegengesteld geladen ionen geeft ionische verbindingen hoge smelt- en kookpunten.
* Kristallijne structuur: Ionische verbindingen vormen een regelmatige, driedimensionale roosterstructuur.
* Geleidbaarheid: Ionische verbindingen geleiden elektriciteit wanneer ze gesmolten of opgelost zijn in water, omdat de ionen vrij kunnen bewegen.
Samenvattend leidt het significante verschil in elektronegativiteit tussen kalium en chloor tot de overdracht van een elektron, resulterend in de vorming van positief en negatief geladen ionen die bij elkaar worden gehouden door sterke elektrostatische krachten, waardoor kaliumchloride een ionische verbinding wordt.
 Zink:het perfecte materiaal voor bioabsorbeerbare stents?
Zink:het perfecte materiaal voor bioabsorbeerbare stents?  Welke verandering is erbij als de waterdamp in vloeibaar water condenseert?
Welke verandering is erbij als de waterdamp in vloeibaar water condenseert?  Vocht uit aardgas verwijderen:een technisch overzicht
Vocht uit aardgas verwijderen:een technisch overzicht  Bereken de HCl-molariteit op basis van de pH:een stapsgewijze handleiding
Bereken de HCl-molariteit op basis van de pH:een stapsgewijze handleiding  Wat is de bindingshoek en moleculaire vorm van siliciumdisulfide?
Wat is de bindingshoek en moleculaire vorm van siliciumdisulfide?
 Landbouwbranden in Brazilië schaden de gezondheid van baby's, een waarschuwing voor de derde wereld
Landbouwbranden in Brazilië schaden de gezondheid van baby's, een waarschuwing voor de derde wereld Ontdekken hoe graslanden ons klimaat hebben veranderd
Ontdekken hoe graslanden ons klimaat hebben veranderd Convectiestromen:hoe hitte de atmosfeer, het weer en het dagelijks leven beïnvloedt
Convectiestromen:hoe hitte de atmosfeer, het weer en het dagelijks leven beïnvloedt  Wat is het verschil tussen levende wezens en niet-wezens?
Wat is het verschil tussen levende wezens en niet-wezens?  De impact van de bodemmicrobiota op de mitigatie van broeikasgassen in tropische bossen
De impact van de bodemmicrobiota op de mitigatie van broeikasgassen in tropische bossen
Hoofdlijnen
- Wat is een soort reproductie wanneer een nieuwe organismen soms meer dan één worden geproduceerd die erfelijk materiaal heeft dat identiek is aan het ouderorganisme?
- Wat hebben we geleerd van het Human Genome Project?
- Onthulling van de Triceratops-houding:een weinig bekend debat onthuld
- Een universele voedsel- en alarmsignaal gevonden in zoogdierbloed
- Hoe zoet het is:nieuw hulpmiddel voor het karakteriseren van plantensuikertransporteurs
- Live hersenactiviteit volgen met de nieuwe NeuBtracker open-source microscoop
- Een nieuw hulpmiddel voor de identificatie van niet-coderend RNA van planten
- Welke structuur wordt alleen aangetroffen in plantencellen en biedt extra stijfheidsondersteuning aan de buitenkant van de cel?
- Hoe wordt opgeslagen suiker in planten genoemd?
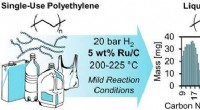
- Een milde manier om plastic in flessen te upcyclen tot brandstof en andere hoogwaardige producten
- Geometrisch verbijsterende quasikristallen gevonden in het puin van de allereerste nucleaire explosie

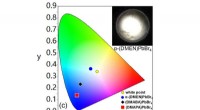
- Door de interne structuur van 2D-hybride perovskietmaterialen te wijzigen, zenden ze wit licht uit
- Inzicht in de gasstroom voor verbeterde toepassingen voor schone energie

- Onderzoekers rapporteren efficiënte platformtechnologie voor de productie van cefalosporine-antibiotica

 Wat zijn de soorten bodems in Agra?
Wat zijn de soorten bodems in Agra?  Hoe halfgeleiderdefecten de kwantumtechnologie een boost kunnen geven
Hoe halfgeleiderdefecten de kwantumtechnologie een boost kunnen geven  Studie:vernietiging door zeespiegelstijging in Californië kan groter zijn dan de ergste bosbranden en aardbevingen
Studie:vernietiging door zeespiegelstijging in Californië kan groter zijn dan de ergste bosbranden en aardbevingen Thianthreniumchemie maakt reactiviteitsverandering van een nucleofiel aminozuur in een veelzijdig tussenproduct mogelijk
Thianthreniumchemie maakt reactiviteitsverandering van een nucleofiel aminozuur in een veelzijdig tussenproduct mogelijk  Kookt vloeibaar helium een fysieke eigenschap?
Kookt vloeibaar helium een fysieke eigenschap?  Wanneer het magnetronsignaal de kromming van de aarde volgt, staat deze bekend als?
Wanneer het magnetronsignaal de kromming van de aarde volgt, staat deze bekend als?  Nieuwe studie toont aan dat arctische opwarming bijdraagt aan droogte
Nieuwe studie toont aan dat arctische opwarming bijdraagt aan droogte NASA schiet naar de maan, op weg naar Mars
NASA schiet naar de maan, op weg naar Mars
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

