
Wetenschap
Pyrrole versus pyridine-basiciteit:het verschil begrijpen
1. Beschikbaarheid van een enkel paar:
* Pyridine: Het stikstofatoom in pyridine heeft een eenzaam elektronenpaar dat is gelokaliseerd in een sp 2 hybride orbitaal. Dit eenzame paar is direct beschikbaar voor donatie aan een proton, waardoor pyridine een sterkere base wordt.
* Pyrrole: Het stikstofatoom in pyrrool heeft een eenzaam elektronenpaar dat is gedelokaliseerd binnen het aromatische ringsysteem. Deze delokalisatie maakt het eenzame paar minder beschikbaar voor donatie, waardoor de basiciteit van pyrrool wordt verminderd.
2. Aromaticiteit:
* Pyrrole: De aromaatiteit van Pyrrool wordt gehandhaafd door de delokalisatie van het vrije stikstofpaar binnen de ring. Het verstoren van deze delokalisatie door protonering zou het molecuul destabiliseren, waardoor protonering minder gunstig wordt.
* Pyridine: De aromaatiteit van pyridine wordt niet beïnvloed door protonering van het vrije stikstofpaar. Dit komt omdat het eenzame paar niet betrokken is bij het aromatische systeem.
3. Resonantie:
* Pyrrole: Resonantiestructuren voor pyrrool laten zien dat het stikstofatoom een gedeeltelijke positieve lading draagt, waardoor het minder waarschijnlijk is dat het een proton accepteert.
* Pyridine: Bij de resonantiestructuren van Pyridine is niet het vrije stikstofpaar betrokken, dus het stikstofatoom behoudt een gedeeltelijke negatieve lading, waardoor het waarschijnlijker wordt een proton te accepteren.
Samengevat:
Het enige paar in pyridine is gemakkelijker beschikbaar voor protonering vanwege de gelokaliseerde aard ervan en het gebrek aan betrokkenheid bij aromatische eigenschappen. Daarentegen maakt het gedelokaliseerde eenzame paar in pyrrool het minder basisch, omdat protonering de aromatiteit en resonantiestabilisatie van het molecuul zou verstoren.
Hoofdlijnen
- Een vroeg kerstcadeau:wetenschappers hebben het rendiergenoom uitgepakt
- Hoe verschillen meiose en mitose?
- De ascomyceten ontlenen hun naam aan welk aspect van de levenscyclus een vegetatieve groeivorm b aseksuele sporenproductie c seksuele structuren d vormen het e-type mycelium?
- Wat zijn celgrenzen?
- Ziet RNA eruit als ladder in tweeën gesneden?
- Welke groep organismen die tegenwoordig levend zijn, lijken het meest op de eerste cellen op aarde?
- Was Tyrannosaurus rex een roofdier of een aaseter?
- Schimmelsporen versus bacteriële endosporen:kernverschillen verklaard
- Wat zijn isostopes?
- Reductie zorgt voor schonere en efficiëntere katalytische reacties

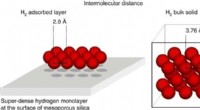
- Superdichte pakking van waterstofmoleculen op een oppervlak
- Massaspectrometrietechniek helpt bij het identificeren van vervalste manuscripten van Robert Burns

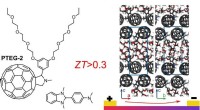
- Warmte omzetten in kracht met efficiënt organisch thermo-elektrisch materiaal
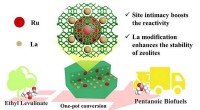
- Nabijheid van actieve sites op maat van zeoliet voor efficiënte productie van pentaan-biobrandstoffen
 Welke planeet is 30 van de zon?
Welke planeet is 30 van de zon?  Hoeveel milligram zijn 300 nanogrammen?
Hoeveel milligram zijn 300 nanogrammen?  Wat is een grote luchtlucht met dezelfde eigenschappen als oppervlak eronder?
Wat is een grote luchtlucht met dezelfde eigenschappen als oppervlak eronder?  Soorten bacteriën leven in zure pH
Soorten bacteriën leven in zure pH  Draagbaar nanovezelapparaat biedt nauwkeurige, point-and-shoot-mogelijkheid
Draagbaar nanovezelapparaat biedt nauwkeurige, point-and-shoot-mogelijkheid Onderzoek kijkt naar wrijvingseigenschappen van materiaal
Onderzoek kijkt naar wrijvingseigenschappen van materiaal Sensoren krijgen een laservorm
Sensoren krijgen een laservorm Conserveringsonderzoek gebruikt kleine loopbanden om het uithoudingsvermogen van de zeeschildpadden te testen
Conserveringsonderzoek gebruikt kleine loopbanden om het uithoudingsvermogen van de zeeschildpadden te testen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


