
Wetenschap
Reactiviteit van het periodiek systeem:de meeste en minst reactieve elementen uitgelegd
Meest reactief:
* Alkalimetalen (Groep 1): Deze elementen hebben slechts één elektron in hun buitenste schil, waardoor ze dit graag willen verliezen en positieve ionen willen vormen. Dit maakt ze ongelooflijk reactief, vooral met water.
* Halogenen (Groep 17): Halogenen hebben zeven elektronen in hun buitenste schil, waardoor ze graag één elektron willen winnen om hun octet te voltooien. Het zijn zeer reactieve niet-metalen en vormen vaak zouten met metalen.
Minst reactief:
* Edelgassen (Groep 18): Deze elementen hebben een volledige buitenste schil van elektronen (acht elektronen, behalve Helium, dat er twee heeft), waardoor ze extreem stabiel en niet-reactief zijn.
Belangrijke opmerkingen:
* Reactiviteitstrends: De reactiviteit binnen groepen neemt over het algemeen toe naarmate u lager in het periodiek systeem komt. Dit komt omdat het buitenste elektron verder van de kern raakt en gemakkelijker kan worden verwijderd of gewonnen.
* Uitzonderingen: Overgangsmetalen (in het midden van het periodiek systeem) hebben vaak een variabele reactiviteit, afhankelijk van het specifieke element en zijn oxidatietoestand.
Samengevat: De alkalimetalen en halogenen zijn de meest reactieve groepen, terwijl de edelgassen het minst reactief zijn.
Hoofdlijnen
- Wanneer het eukaryotische celgedeelte richtingen bevat voor groei en reproductie?
- Waarom zijn transmissiepositie microscopen en akoestische belangrijke hulpmiddelen om te begrijpen hoe levende cellen functioneren?
- Het soort genen dat een organisme bezit, is afhankelijk van wat?
- Wat is de definitie van merk -DNA?
- Waarom is communicatie tussen wetenschappers belangrijk?
- De rol van fruit bij de voortplanting van angiospermen:bescherming en zaadverspreiding
- Celmembraan en homeostase:cellulaire controle begrijpen
- Welk instrument wordt gebruikt om het karakter van de ademhaling vast te stellen?
- Stervende zalm brengt de enorme viskwekerijindustrie van Noorwegen in moeilijkheden
- Ingenieurs maken veelbelovend materiaal stabiel genoeg voor gebruik in zonnecellen

- Een harig forensisch probleem oplossen
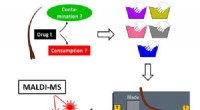
- Door bacteriële enzymen te kopiëren, lab leert snel nieuwe klasse antibiotica moleculen schoon te synthetiseren, efficiënt

- Video:Rijdt uw brandstofcelauto... op benzine?

- Duurzame bioplastics maken van elektriciteitsetende microben

 Wat is de betekenis van de aarde in de Romeinse mythologie?
Wat is de betekenis van de aarde in de Romeinse mythologie?  Waarom reflecteert enceladus zoveel licht?
Waarom reflecteert enceladus zoveel licht?  Eerste succesvolle laservangst van cirkelvormige Rydberg-atomen
Eerste succesvolle laservangst van cirkelvormige Rydberg-atomen Instrument wordt gebruikt om vloeistoffen afzonderlijke componenten te draaien?
Instrument wordt gebruikt om vloeistoffen afzonderlijke componenten te draaien?  Onderzoekers creëren negende manier om een batterij te doden
Onderzoekers creëren negende manier om een batterij te doden Onderzoekers bereiken extreem-ultraviolette spectrale compressie door vier-golfmenging
Onderzoekers bereiken extreem-ultraviolette spectrale compressie door vier-golfmenging Leren over liefde via online dating
Leren over liefde via online dating Welke bronnen gebruiken om energie te leveren?
Welke bronnen gebruiken om energie te leveren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


