
Wetenschap
Hydrofobe moleculen:een uitgebreide lijst en categorisering
Hydrofobe moleculen:een lijst
Het is belangrijk op te merken dat hydrofobiciteit een relatieve eigenschap is, en geen absolute. De hydrofobiciteit van een molecuul kan variëren afhankelijk van de omgeving en de andere aanwezige moleculen.
Hier is een lijst met moleculen die over het algemeen als hydrofoob worden beschouwd, gecategoriseerd op basis van hun chemische aard:
1. Koolwaterstoffen:
* Alkanen: Methaan, Ethaan, Propaan, Butaan, Pentaan, Hexaan, Heptaan, Octaan, Nonaan, Decaan
* Alkenen: Etheen, Propeen, Buteen, Penteen, Hexeen
* Alkynen: Ethyne, Propyn, Butyn, Pentyne
* Aromatische koolwaterstoffen: Benzeen, Tolueen, Xyleen
2. Lipiden:
* Vetten: Triglyceriden, Fosfolipiden (staarten), Cholesterol
* Wassen: Bijenwas, Carnaubawas
* Steroïden: Testosteron, oestrogeen, cortisol
3. Gassen:
* Stikstof (N2)
* Zuurstof (O2)
* Kooldioxide (CO2)
* Helium (Hij)
* Neon (Ne)
* Argon (Ar)
* Krypton (Kr)
* Xenon (Xe)
4. Anders:
* Chloorfluorkoolwaterstoffen (CFK's)
* Polytetrafluorethyleen (PTFE) (Teflon)
* Siliconenoliën
* Paraffine
5. Biologische moleculen:
* Aminozuren: Alanine, Valine, Leucine, Isoleucine, Proline, Fenylalanine, Tryptofaan, Methionine
* Eiwitten: Veel eiwitten hebben hydrofobe gebieden die betrokken zijn bij de vouwing en interacties van eiwitten.
Opmerking:
* Dit is geen uitputtende lijst en er zijn veel andere hydrofobe moleculen.
*De mate van hydrofobiciteit varieert binnen elke categorie.
* Sommige moleculen kunnen zowel hydrofobe als hydrofiele gebieden hebben, waardoor ze amfipatisch zijn.
Voor een beter begrip van hydrofobiciteit is het belangrijk om het volgende te overwegen:
* Moleculaire structuur: Niet-polaire moleculen met een hoog aandeel C-H-bindingen hebben de neiging hydrofoob te zijn.
* Intermoleculaire krachten: Hydrofobe moleculen hebben een zwakke interactie met water en een sterke interactie met elkaar.
* Oplosmiddeleigenschappen: Hydrofobe moleculen zijn beter oplosbaar in niet-polaire oplosmiddelen zoals olie of hexaan.
Het begrijpen van hydrofobiciteit is op veel gebieden essentieel, waaronder:
* Biologie: Celmembranen, eiwitvouwing, medicijnafgifte
* Chemie: Selectie van oplosmiddelen, reacties, materiaalkunde
* Milieuwetenschappen: Vervuiling, waterzuivering, klimaatverandering
* Geneeskunde: Geneesmiddelenontwerp, farmaceutische formulering
* Voedingswetenschap: Emulsies, conservering van voedsel
 Bij welke druk wordt lachgas vloeibaar?
Bij welke druk wordt lachgas vloeibaar?  Wat betekenen de symbolen en het getal in chemische formule van een ionische verbinding?
Wat betekenen de symbolen en het getal in chemische formule van een ionische verbinding?  Hoeveel naionen zijn er in 4,2 g NaCl?
Hoeveel naionen zijn er in 4,2 g NaCl?  Het ontrafelen van de geschiedenis en wetenschap achter oude decoratieve metalen draden
Het ontrafelen van de geschiedenis en wetenschap achter oude decoratieve metalen draden Wat is de formule voor verbinding gevormd door Barium Ion BA2 en Hydroxide OH?
Wat is de formule voor verbinding gevormd door Barium Ion BA2 en Hydroxide OH?
 Voetbalveld regenwoud vernietigd elke zes seconden
Voetbalveld regenwoud vernietigd elke zes seconden De ijskap van Perus Quelccaya zou tegen het midden van de jaren 2050 kunnen verdwijnen
De ijskap van Perus Quelccaya zou tegen het midden van de jaren 2050 kunnen verdwijnen Rood tij rollen:Schadelijke algen blijken te gedijen in zowel hoge, omgevingen met weinig CO2
Rood tij rollen:Schadelijke algen blijken te gedijen in zowel hoge, omgevingen met weinig CO2 Uit onderzoek blijkt hoe invasieve ondergedompelde macrofyten de stikstofcyclus in het sediment onder complexe omgevingen beïnvloeden
Uit onderzoek blijkt hoe invasieve ondergedompelde macrofyten de stikstofcyclus in het sediment onder complexe omgevingen beïnvloeden  Realtime gegevens tonen de enorme impact van COVID-19 op de wereldwijde emissies
Realtime gegevens tonen de enorme impact van COVID-19 op de wereldwijde emissies
Hoofdlijnen
- DNA-replicatie:waarom is het essentieel voor mitose en meiose?
- Uit onderzoek blijkt hoe een 'Zwitsers zakmes'-eiwit fagen helpt hun slachtoffers te ontwapenen
- Wat neemt toe wanneer een cel zich in twee kleinere cellen verdeelt?
- Welke organel is verantwoordelijk voor de energieproductie in cel?
- Substraatmoleculen binden aan enzymen waar?
- Zowel planten- als diercellen hebben mitochondriën omdat ze allebei?
- Kankerbiologen vinden een sleutel die kan ontsluiten hoe tumoren zich vormen en zich ontwikkelen
- Wat is een tweede neef? Het ontrafelen van de stamboom
- Wat is een voorbeeld van een basale metabolisme -activiteit?
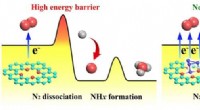
- Het bereiken van een zeer efficiënte ammoniaksynthese door de snelheidsbepalende stap te wijzigen
- Nieuwe antivirale, antibacterieel oppervlak kan de verspreiding van infecties in ziekenhuizen verminderen

- Hier is een draai aan een eeuwenoude klassieker:Lactosevrije chocolademelk

- Chemici melden biohernieuwbaar, biologisch afbreekbaar plastic alternatief

- Zullen cyborgs gemaakt worden van melanine? Pigmentdoorbraak maakt biocompatibele elektronica mogelijk
 Hoe technologie het platteland van Zuid-Afrika kan helpen zonneschijn in inkomen te veranderen
Hoe technologie het platteland van Zuid-Afrika kan helpen zonneschijn in inkomen te veranderen Kan de impuls van kracht nul zijn, zelfs niet nul?
Kan de impuls van kracht nul zijn, zelfs niet nul?  Wat is een materiaal dat elektronen draagt?
Wat is een materiaal dat elektronen draagt?  Hoe kan een golf energie verplaatsen en er niet toe doen?
Hoe kan een golf energie verplaatsen en er niet toe doen?  Wat is een kracht die in tegengestelde richtingen wordt getrokken?
Wat is een kracht die in tegengestelde richtingen wordt getrokken?  Wat is Ozone en CO2 zijn ze hetzelfde?
Wat is Ozone en CO2 zijn ze hetzelfde?  Een rots wordt gedropt van een hoogte van 30 m en in vrije herfst Wat de snelheid als deze 2,5 seconden later grond bereikt?
Een rots wordt gedropt van een hoogte van 30 m en in vrije herfst Wat de snelheid als deze 2,5 seconden later grond bereikt?  COVID-19 politiek commentaar gekoppeld aan online haatmisdrijven
COVID-19 politiek commentaar gekoppeld aan online haatmisdrijven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

