
Wetenschap
Covalente bindingen in water:stabiliteit en dissociatie
Dit is waarom:
* Covalente bindingen zijn sterk: Covalente bindingen omvatten het delen van elektronen tussen atomen. Deze gedeelde elektronen creëren een sterke aantrekkingskracht tussen de atomen en houden ze bij elkaar.
* Water is een polair oplosmiddel: Watermoleculen hebben een gedeeltelijk positieve lading op de waterstofatomen en een gedeeltelijk negatieve lading op het zuurstofatoom. Door deze polariteit kan water interageren met ionische verbindingen en polaire moleculen, maar het heeft doorgaans niet genoeg kracht om covalente bindingen te verbreken.
Er zijn echter uitzonderingen aan deze regel:
* Zwakke covalente bindingen: Sommige covalente bindingen, vooral die met lage elektronegativiteitsverschillen tussen de atomen, kunnen door water worden verbroken. De bindingen in sommige carbonzuren kunnen bijvoorbeeld gedeeltelijk dissociëren in water, wat leidt tot het vrijkomen van H+-ionen en de vorming van carboxylaationen.
* Hydrolyse: Bepaalde covalente bindingen kunnen door water worden verbroken via een proces dat hydrolyse wordt genoemd. Dit omvat de toevoeging van een watermolecuul aan de binding, waardoor deze wordt verbroken en twee nieuwe moleculen worden gevormd. Door de hydrolyse van sucrose (tafelsuiker) wordt deze bijvoorbeeld afgebroken tot glucose en fructose.
* Zuur-base-reacties: Sterke zuren zoals zoutzuur (HCl) kunnen protonen (H+) aan water doneren, waardoor de covalente binding in het HCl-molecuul wordt verbroken. Dit leidt tot de vorming van hydroniumionen (H3O+) en chloride-ionen (Cl-), waardoor het HCl-molecuul in water effectief wordt gedissocieerd.
Samengevat:
Covalente bindingen zijn over het algemeen erg sterk en dissociëren niet gemakkelijk in water. Er zijn echter uitzonderingen waarbij sprake is van zwakke covalente bindingen, hydrolysereacties en sterke zuur-base-reacties.
Hoofdlijnen
- De code van colibactine kraken:studie onderzoekt hoe de verbinding het DNA beschadigde om het verband met kanker te begrijpen
- Wat doet de kern van een cel?
- Wat is de functie van anastomoses?
- Wat zijn de verschillen en overeenkomsten tussen prokaryotische eukadyotische cellen?
- Wat is een groep cellen die speciale chemicaliën voor je lichaam maken?
- Wat gebeurt er als twee verschillende soorten proberen dezelfde niche te bezetten?
- Wat zijn de celorganellen gevuld met enzymen die nodig zijn om bepaalde materialen in cel af te breken?
- Wat is de chemische vergelijking voor aërobe ademhaling?
- Wat is het deel van de cel dat chlorofyl bevat?
- Nieuwe technologie voltooit vitale klasse van industriële reacties vijf keer sneller

- Model voor op 2D materiaal gebaseerde RRAM gevonden

- Onderzoekers lossen eiwitstructuur op die verband houdt met erfelijke netvliesaandoeningen
- Kalium geeft op perovskiet gebaseerde zonnecellen een efficiëntieboost

- Ontwikkeld enzym dat PET in tien uur kan afbreken
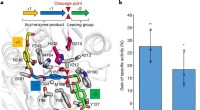
 Wat kunnen bacteriën graag vinden voor de lunch?
Wat kunnen bacteriën graag vinden voor de lunch?  Welke structuur maakt het mogelijk om enorme DNA -lengtes in de kern te vouwen?
Welke structuur maakt het mogelijk om enorme DNA -lengtes in de kern te vouwen?  Which color star has the lowest surface temperature?
Which color star has the lowest surface temperature?  Cathay Pacific koopt budgetluchtvaartmaatschappij HK Express voor $ 628 miljoen
Cathay Pacific koopt budgetluchtvaartmaatschappij HK Express voor $ 628 miljoen Als een auto een massa van 1000 kg heeft. Wat is de versnelling geproduceerd met geweld 2000 N?
Als een auto een massa van 1000 kg heeft. Wat is de versnelling geproduceerd met geweld 2000 N?  Waar is de locatie van Spacelab in de lucht?
Waar is de locatie van Spacelab in de lucht?  Aas van Pentakels:ontsluiten van de rijkdom aan kansen
Aas van Pentakels:ontsluiten van de rijkdom aan kansen  Tatoeages op nanoschaal voor individuele cellen kunnen vroegtijdige waarschuwingen geven voor gezondheidsproblemen
Tatoeages op nanoschaal voor individuele cellen kunnen vroegtijdige waarschuwingen geven voor gezondheidsproblemen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


