
Wetenschap
Isotone oplossingen:identificatie en meting
Zo kun je vaststellen of twee oplossingen isotoon zijn:
1. Osmotische druk rechtstreeks meten:
* Bij deze methode wordt gebruik gemaakt van een osmometer, een apparaat dat de druk meet die nodig is om de waterstroom door een semipermeabel membraan te voorkomen.
*Als de osmotische druk van de twee oplossingen hetzelfde is, zijn ze isotoon.
2. Vergelijking van de concentratie van opgeloste stoffen:
* Voor niet-elektrolytoplossingen: Als de concentratie van opgeloste stoffen (in termen van molariteit of molaliteit) in beide oplossingen hetzelfde is, zijn ze isotoon.
* Voor elektrolytoplossingen: U moet rekening houden met de dissociatie van elektrolyten. Een 1 M oplossing van NaCl zal bijvoorbeeld tweemaal de osmotische druk hebben van een 1 M oplossing van glucose, omdat NaCl dissocieert in twee ionen (Na+ en Cl-).
* Effectieve osmolariteit berekenen: Om elektrolytoplossingen te vergelijken, berekent u de effectieve osmolariteit, waarbij rekening wordt gehouden met het aantal deeltjes dat door dissociatie wordt geproduceerd. Bijvoorbeeld:
* 1 M NaCl-oplossing heeft een osmolariteit van 2 Osm (1 M Na+ + 1 M Cl-)
* 1 M glucose-oplossing heeft een osmolariteit van 1 Osm (1 M glucose)
* Als de effectieve osmolariteit voor beide oplossingen hetzelfde is, zijn ze isotoon.
3. Celgedrag observeren:
* Experiment met rode bloedcellen: Plaats rode bloedcellen in elk van de oplossingen.
*Als de cellen onveranderd blijven, zijn de oplossingen isotoon.
* Als de cellen krimpen, is de oplossing hypertoon (hogere concentratie opgeloste stoffen).
* Als de cellen opzwellen of barsten, is de oplossing hypotoon (lagere concentratie opgeloste stoffen).
Belangrijke overwegingen:
* Temperatuur: Osmotische druk wordt beïnvloed door de temperatuur. Zorg ervoor dat beide oplossingen dezelfde temperatuur hebben wanneer u ze vergelijkt.
* Type membraan: De permeabiliteit van het semipermeabele membraan kan ook de beweging van water beïnvloeden. Zorg ervoor dat u voor uw experiment hetzelfde type membraan gebruikt.
Samenvattend:om te bepalen of twee oplossingen isotoon zijn, kunt u rechtstreeks hun osmotische druk meten, de concentratie van opgeloste stoffen vergelijken (rekening houdend met dissociatie) of het gedrag observeren van cellen die in elke oplossing zijn geplaatst.
 Laos zet door met verwoestende nieuwe dam op Mekong
Laos zet door met verwoestende nieuwe dam op Mekong Wat is het terrein van het regenwoud?
Wat is het terrein van het regenwoud?  Grootschalig experiment op het landelijke Olympisch schiereiland om innovaties in bosbeheer te testen
Grootschalig experiment op het landelijke Olympisch schiereiland om innovaties in bosbeheer te testen Wanneer fracking de buurt intrekt, geestelijke gezondheidsrisico's nemen toe
Wanneer fracking de buurt intrekt, geestelijke gezondheidsrisico's nemen toe Hoe het verbieden van plastic tassen New York kan helpen de klimaatverandering te verminderen
Hoe het verbieden van plastic tassen New York kan helpen de klimaatverandering te verminderen
Hoofdlijnen
- Onderzoekers willen weten waarom beluga-walvissen zich niet hebben hersteld
- Wat is het gelei -materiaal buiten de kern?
- Door een gekoesterd fossiel te doneren aan de specimenverzameling, werkt wetenschapper samen met andere onderzoekers, wat verklaart het beste waarom dit misschien waar is?
- Voor duurzame vliegtuigbrandstof ontwikkelen onderzoekers een veelbelovend micro-organisme voor de productie van precursoren
- Wat is het organisme dat zowel mannelijke als vrouwelijke structuren heeft genoemd?
- Wat is een term die beschrijft waarom sommige individuen meer nakomelingen produceren dan anderen?
- Hoe verwerven cellen homologe chromosoomparen die de allelen dragen, onafhankelijk diverteren?
- Wat betekenen wetenschappers met nieuwe soorten?
- Wilgenroosje:de roze pionier
- Voedingsvezels helpen materiaal in je darmen te klonteren
- Hoe u de pH-waarde van water veilig kunt verhogen met zuiveringszout en andere alkalische additieven

- De chemische eigenschappen van citroensap:zuurgraad, vitamine C en antimicrobiële voordelen

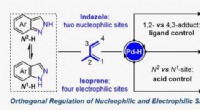
- Orthogonale regulatiestrategie biedt nieuwe kansen voor opbouw van moleculaire complexiteit
- Onderzoekers realiseren de ideale elektronische structuur van kagome-metaal

 Hoeveel ethylalcohol bevat wrijven?
Hoeveel ethylalcohol bevat wrijven?  Waarom worden wolken donker als het gaat stormen?
Waarom worden wolken donker als het gaat stormen?  Hoe heet een groep pulserende sterren?
Hoe heet een groep pulserende sterren?  Wat is een symbool voor versnelling?
Wat is een symbool voor versnelling?  112 graden Fahrenheit Wat is het Celsius?
112 graden Fahrenheit Wat is het Celsius?  Zijn millennials genderrebellen of keren ze terug naar de traditie?
Zijn millennials genderrebellen of keren ze terug naar de traditie?  Lasers zappen ontsmet van bodem
Lasers zappen ontsmet van bodem Exxon Mobils ommezwaai over klimaatonthulling
Exxon Mobils ommezwaai over klimaatonthulling
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

