
Wetenschap
Hoe katalyseert enzymen een chemische reactie?
1. Substraatbinding:
* Enzymen hebben specifieke actieve locaties, regio's met een unieke vorm en chemische omgeving.
* Het substraat, het molecuul waarop het enzym werkt, bindt aan de actieve plaats en vormt een enzym-substraatcomplex.
* Deze binding is zeer specifiek, zoals een slot en sleutel, waardoor het enzym alleen de gewenste reactie katalyseert.
2. Activeringsenergie verlagen:
* Eenmaal gebonden, kan het enzym het substraatmolecuul belasten, waardoor bestaande bindingen worden verzwakt.
* Het kan ook reactieve groepen dichter bij elkaar brengen, waardoor de vorming van nieuwe obligaties wordt vergemakkelijkt.
* Door de chemische omgeving van de actieve locatie te wijzigen, creëert het enzym een overgangstoestand, een energierijke tussenliggende toestand die nodig is om de reactie door te gaan.
* Deze overgangstoestand heeft een lagere energie dan die zonder het enzym, waardoor de activeringsenergiebarrière effectief wordt verlaagd.
3. Productvorming en release:
* De reactie treedt op en vormt het product.
* Het product heeft een lagere affiniteit voor de actieve site dan het substraat en wordt vrijgegeven.
* Het enzym blijft ongewijzigd en is klaar om een ander substraatmolecuul te binden, waardoor de reactie opnieuw katalyseert.
Samenvattend:
Enzymen versnellen reacties door:
* Biedt een alternatieve reactieroute met een lagere activeringsenergie.
* het stabiliseren van de overgangstoestand, waardoor het gemakkelijker te bereiken is.
* het verhogen van de frequentie van botsingen tussen reactanten.
Voorbeelden:
* lactase: Breekt lactose, een suiker in melk, af in eenvoudiger suikers.
* amylase: Breekt zetmeel af in eenvoudiger suikers.
* DNA -polymerase: Katalyseert de synthese van DNA -moleculen.
factoren die de enzymactiviteit beïnvloeden:
* Temperatuur: Enzymen hebben een optimale temperatuur voor activiteit.
* pH: Elk enzym heeft een optimaal pH -bereik voor activiteit.
* Substraatconcentratie: De reactiesnelheid neemt toe met de substraatconcentratie totdat verzadiging is bereikt.
* remmers: Moleculen die aan het enzym kunnen binden en zijn activiteit kunnen blokkeren.
Inzicht in hoe enzymen reacties katalyseren, is cruciaal op velden zoals geneeskunde, biotechnologie en voedselwetenschap. Ze spelen een cruciale rol in alle biologische processen, van digestie tot energieproductie.
 Is een CO2 in waterelementmengsel of -verbinding?
Is een CO2 in waterelementmengsel of -verbinding?  Welke concentratie van een oplossing CH3OH in water heeft het laagste vriespunt?
Welke concentratie van een oplossing CH3OH in water heeft het laagste vriespunt?  Wat is een wetenschappelijk woord voor buitenlandse chemicaliën?
Wat is een wetenschappelijk woord voor buitenlandse chemicaliën?  Hoeveel mol is 2.17x10 Representatieve broomdeeltjes?
Hoeveel mol is 2.17x10 Representatieve broomdeeltjes?  Hoe beïnvloedt zout het smelt- en vriespunt van water?
Hoe beïnvloedt zout het smelt- en vriespunt van water?
 Wat zijn de negatieve gevolgen van natuurrampen?
Wat zijn de negatieve gevolgen van natuurrampen?  Hoe speelt water een rol bij het vormgeven van het aardoppervlak?
Hoe speelt water een rol bij het vormgeven van het aardoppervlak?  Er kan een enorme fout zijn in de hoop op fracking in het VK - de geologie
Er kan een enorme fout zijn in de hoop op fracking in het VK - de geologie Bijna de helft van de Californische vegetatie loopt gevaar door klimaatstress
Bijna de helft van de Californische vegetatie loopt gevaar door klimaatstress Californië bosbrand fakkelt bos, dwingt nieuwe evacuaties af
Californië bosbrand fakkelt bos, dwingt nieuwe evacuaties af
Hoofdlijnen
- Ontdekken hoe microben samenwerken
- Wat is een biocapaciteit?
- Hoeveel verschillende celtypen zijn er in het menselijk lichaam?
- Wat is de fysiologische definitie van STEM?
- Welk deel van de plantencel wordt gedeeld door dierencellen?
- Hoe bacteriën zichzelf vaccineren tegen virale indringers
- Hoe heeft de uitvinding van de microscoop de celtheorie beïnvloed?
- Voors en tegens van Cloning Plants & Animals
- Wat is het verschil tussen een clade en taxon?
- Cryo-elektronenmicroscopie onthult gemeenschappelijke herpesvirusstructuur
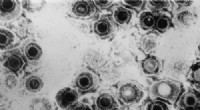
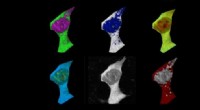
- Alzheimerziekte zorgt ervoor dat cellen oververhit raken en bakken als eieren
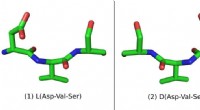
- Door de spiegel:nieuwe spiegelbeeldmoleculen kunnen leiden tot betere medicijnen
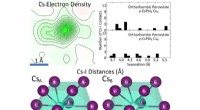
- Chemici lossen de oorsprong van perovskietinstabiliteit op
- NIST presenteert eerste real-world test van nieuwe sensorontwerpen voor schoorsteenemissies

 Energiestroom en chemische cyclus door Ecosystem
Energiestroom en chemische cyclus door Ecosystem Wat wordt kracht uitgeoefend tegen iets?
Wat wordt kracht uitgeoefend tegen iets?  Hoe wordt LDPE gerecycled?
Hoe wordt LDPE gerecycled?  Twee manieren om optische waarneming te verbeteren met verschillende resonatortechnieken
Twee manieren om optische waarneming te verbeteren met verschillende resonatortechnieken Opinie:Vakbonden kunnen en zullen een leidende rol spelen bij de aanpak van de klimaatcrisis
Opinie:Vakbonden kunnen en zullen een leidende rol spelen bij de aanpak van de klimaatcrisis Waarom is een uniforme lineaire beweging geen versnelde beweging?
Waarom is een uniforme lineaire beweging geen versnelde beweging?  Hoe heet de verspilde energie?
Hoe heet de verspilde energie?  United sluit zich aan bij Southwest, Amerikaan in nieuwe 737 MAX vertraging
United sluit zich aan bij Southwest, Amerikaan in nieuwe 737 MAX vertraging
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

