
Wetenschap
Zijn niet-polaire moleculen meer aangetrokken tot andere of polaire moleculen?
* intermoleculaire krachten: De krachten die moleculen bij elkaar houden, worden intermoleculaire krachten genoemd. Niet-polaire moleculen interageren voornamelijk via zwakke dispersiekrachten in Londen, die voortkomen uit tijdelijke fluctuaties in elektronenverdeling. Polaire moleculen hebben daarentegen sterkere dipool-dipoolinteracties en soms waterstofbinding.
* Oplosbaarheid: "Zoals oplost zoals" is een goede vuistregel. Niet-polaire moleculen zullen beter oplossen in niet-polaire oplosmiddelen, terwijl polaire moleculen beter oplossen in polaire oplosmiddelen. Dit komt omdat de intermoleculaire krachten tussen vergelijkbare moleculen sterker zijn, waardoor een betere menging mogelijk is.
Voorbeeld:
* olie en water: Olie is niet-polair en water is polair. Ze mengen niet goed omdat de sterke waterstofbindingen in water niet gemakkelijk worden verstoord door de zwakke dispersiekrachten in Londen in olie.
Samenvattend: Niet-polaire moleculen worden aangetrokken door andere niet-polaire moleculen vanwege de zwakkere, maar nog steeds aanwezige, Londense dispersiekrachten.
 Klimaatverandering zorgt voor hevigere stormen in heel Europa
Klimaatverandering zorgt voor hevigere stormen in heel Europa NASA-satelliet vindt tropische cycloon Marcus in de buurt van de Australische kust van Cobourg Peninsula
NASA-satelliet vindt tropische cycloon Marcus in de buurt van de Australische kust van Cobourg Peninsula De aardbeving in Kaikoura kan ertoe leiden dat de modellen voor aardbevingsgevaar internationaal worden heroverwogen
De aardbeving in Kaikoura kan ertoe leiden dat de modellen voor aardbevingsgevaar internationaal worden heroverwogen Waarom worden orkanen zwakker als ze het land raken?
Waarom worden orkanen zwakker als ze het land raken?  De kust doseren:de lekkende leidingen van Baltimore County genezen de Chesapeake Bay
De kust doseren:de lekkende leidingen van Baltimore County genezen de Chesapeake Bay
Hoofdlijnen
- Biologen ontdekken genetische routes die het immuunsysteem en de bloedsomloop van muggen tijdens infectie met elkaar verbinden
- Wat zijn drie manieren waarop soorten zich kunnen verspreiden?
- Syngenta schikt Amerikaanse boerenrechtszaken in Chinese maïshandelzaak
- Wat is bacteriën geclassificeerd?
- De Filippijnse bioloog en hun bijdragen?
- De verschillende tropismen in planten worden veroorzaakt door gelokaliseerde gebieden van snellere cel Wat?
- Wat zijn twee voorbeelden van hoe anaërobe ademhaling wordt gebruikt in de voedsel- en drankenindustrie?
- Wat is microbiolagy?
- Cellen met een kern- en membraangebonden organellen?
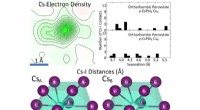
- Chemici lossen de oorsprong van perovskietinstabiliteit op
- Ingenieurs hergebruiken wespengif als antibioticum

- Papier of plastic? Stijve waterdichte coating voor papier is bedoeld om onze afhankelijkheid van plastic te verminderen

- Terwijl deze bacteriën eten, genereren ze een ongebruikelijk driehoekig molecuul dat kan worden gebruikt om vliegtuigbrandstof te maken
- De kloof op nanoschaal overbruggen:een diepe blik in atomaire schakelaars
 Welke maat ster heeft het langste leven?
Welke maat ster heeft het langste leven?  EPA-regel beperkt HFK's scherp, gassen gebruikt als koelmiddel
EPA-regel beperkt HFK's scherp, gassen gebruikt als koelmiddel Hoe verschillen algen van andere planten?
Hoe verschillen algen van andere planten?  Gebruikt een snel bewegende stroom energie?
Gebruikt een snel bewegende stroom energie?  Welke sterren zijn de slimste in het sterrenbeeld van kanker?
Welke sterren zijn de slimste in het sterrenbeeld van kanker?  Hoe mW te converteren naar mA
Hoe mW te converteren naar mA  Hoe zou u een magnetron voor een alien beschrijven?
Hoe zou u een magnetron voor een alien beschrijven?  Wat zijn de belangrijkste metabolische afvalproducten?
Wat zijn de belangrijkste metabolische afvalproducten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

