
Wetenschap
Is een methylgroep meer polair dan hydroxylgroep?
Dit is waarom:
* elektronegativiteit: Zuurstof is veel elektronegatiefer dan koolstof en waterstof. Dit betekent dat het elektronen sterker aantrekt, waardoor een gedeeltelijke negatieve lading ontstaat op het zuurstofatoom en een gedeeltelijke positieve lading op het waterstofatoom in de hydroxylgroep.
* polariteit: Het verschil in elektronegativiteit tussen zuurstof en waterstof creëert een significant dipoolmoment in de hydroxylgroep, waardoor het een polaire functionele groep is.
* methylgroep: De methylgroep, met zijn koolstof- en waterstofatomen, heeft zeer vergelijkbare elektronegativiteitswaarden. Dit resulteert in een veel kleiner, bijna verwaarloosbaar dipoolmoment, waardoor het niet -polair is.
Samenvattend: De hydroxylgroep is zeer polair vanwege het elektronegatieve zuurstofatoom, terwijl de methylgroep niet -polair is vanwege zijn vergelijkbare elektronegativiteitswaarden.
 Vertegenwoordigt Kolbe -formule een verbinding?
Vertegenwoordigt Kolbe -formule een verbinding?  Wat is de gebalanceerde neutralisatiereactie tussen H2SO4 en KOH in waterige oplossing?
Wat is de gebalanceerde neutralisatiereactie tussen H2SO4 en KOH in waterige oplossing?  Wat is het product van de reactie van water en een niet -metaal oxide?
Wat is het product van de reactie van water en een niet -metaal oxide?  Nieuw ontwikkelde COVID-19-test detecteert en identificeert specifieke varianten met 100% nauwkeurigheid
Nieuw ontwikkelde COVID-19-test detecteert en identificeert specifieke varianten met 100% nauwkeurigheid Hoeveel mogelijke structuren van trichloorbenzeen?
Hoeveel mogelijke structuren van trichloorbenzeen?
 Onderzoekers suggereren dat rampen met kolenas en residudammen kunnen worden voorkomen
Onderzoekers suggereren dat rampen met kolenas en residudammen kunnen worden voorkomen De ongelijkheid in blootstelling aan luchtvervuiling blijft bestaan in Massachusetts
De ongelijkheid in blootstelling aan luchtvervuiling blijft bestaan in Massachusetts Door welke structuren verkrijgen planten het grootste deel van hun water?
Door welke structuren verkrijgen planten het grootste deel van hun water?  Satellietonderzoek vindt grote verschuivingen in zoetwater wereldwijd
Satellietonderzoek vindt grote verschuivingen in zoetwater wereldwijd Iedereen op jacht naar het element lithium
Iedereen op jacht naar het element lithium
Hoofdlijnen
- Wat wordt gevormd wanneer cellen van hetzelfde type samenvoegen om een gemeenschappelijke taak uit te voeren?
- Hoe tardigrades vriestemperaturen overleven
- Hoe wordt een cel geconstrueerd?
- Beschrijf hoe de ontwikkeling van de celtheorie aantoont dat wetenschappelijke overtuigingen in de loop van de tijd gebruik kunnen maken van specifieke voorbeelden.
- Wat dachten wetenschappers in de zeventiende eeuw dat weefsel betekende?
- Onderzoekers beschrijven hoe duplicaties van DNA-segmenten het 3D-structuurgenoom beïnvloeden
- Wat zijn de kenmerken van iets in domeinbacteriën?
- Hoe veranderen genomen van soorten?
- Wat is biolumineus betekent?
- Lagere uitstoot van kooldioxide in het verschiet voor cement

- Een eiwit dat zichzelf repliceert

- Raamwerkdiversiteit van koolstofnitrides biedt een rijk platform voor katalyse met één atoom

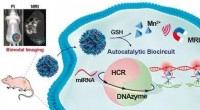
- Amplificatie en beeldvorming van microRNA als biomarker om tumorontwikkeling te detecteren
- Een methode om verborgen serienummers van polymeerproducten te herstellen

 Onderzoek vindt dat aardbevingen systematisch andere kunnen veroorzaken aan de andere kant van de aarde
Onderzoek vindt dat aardbevingen systematisch andere kunnen veroorzaken aan de andere kant van de aarde Wat het materiaal door welke licht reist?
Wat het materiaal door welke licht reist?  Wat voor soort energie gebruikt diffusie?
Wat voor soort energie gebruikt diffusie?  Waarom is het belangrijk om naar meer dan één bron te kijken wanneer u een wetenschappelijk probleem onderzoekt?
Waarom is het belangrijk om naar meer dan één bron te kijken wanneer u een wetenschappelijk probleem onderzoekt?  Een menselijke cel die geen kern heeft?
Een menselijke cel die geen kern heeft?  Wat is een groot deel van het platte of voorzichtig hellend land?
Wat is een groot deel van het platte of voorzichtig hellend land?  Wat hebben alle organismen?
Wat hebben alle organismen?  Lijst met verschillende voorbeelden van eukaryoten
Lijst met verschillende voorbeelden van eukaryoten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

