
Wetenschap
Hoe zijn de eigenschappen van een gas anders dan vloeistof of soild?
gassen
* Vorm en volume: Gassen hebben geen vaste vorm of volume. Ze nemen de vorm en het volume van hun container aan. Dit komt omdat de deeltjes in een gas ver uit elkaar liggen en vrij bewegen.
* Compressibiliteit: Gassen zijn zeer samendrukbaar. Je kunt veel gas in een kleinere ruimte persen.
* Dichtheid: Gassen hebben lage dichtheden in vergelijking met vloeistoffen en vaste stoffen.
* diffusie: Gassen diffunderen gemakkelijk. Ze verspreiden zich om de hele ruimte die ze innemen te vullen.
* intermoleculaire krachten: De krachten van aantrekkingskracht tussen gasmoleculen zijn erg zwak. Hierdoor kunnen ze vrij en onafhankelijk bewegen.
vloeistoffen
* Vorm en volume: Vloeistoffen hebben een vast volume maar nemen de vorm van hun container. Ze stromen en kunnen worden gegoten.
* Compressibiliteit: Vloeistoffen zijn veel minder samendrukbaar dan gassen, maar meer samendrukbaar dan vaste stoffen.
* Dichtheid: Vloeistoffen hebben hogere dichtheden dan gassen, maar lager dan vaste stoffen.
* diffusie: Vloeistoffen diffunderen, maar langzamer dan gassen.
* intermoleculaire krachten: Vloeistoffen hebben sterkere intermoleculaire krachten dan gassen, maar zwakker dan vaste stoffen.
vaste stoffen
* Vorm en volume: Vaste stoffen hebben een vaste vorm en volume. Ze zijn rigide en stromen niet.
* Compressibiliteit: Vaste stoffen zijn erg moeilijk te comprimeren.
* Dichtheid: Vaste stoffen hebben de hoogste dichtheden van de drie staten van materie.
* diffusie: Vaste stoffen verspreiden extreem langzaam, vaak niet detecteerbaar bij normale temperaturen.
* intermoleculaire krachten: Vaste stoffen hebben de sterkste intermoleculaire krachten. Dit houdt hun deeltjes in een vaste, rigide structuur.
Een nuttige analogie:
Denk aan een klaslokaal vol studenten:
* gas: Studenten die wild rondrennen, elkaar tegen het lijf lopen, gaan waar ze maar willen.
* vloeistof: Studenten die dicht bij elkaar staan, kunnen bewegen maar in de klas blijven.
* solide: Studenten die in een vaste formatie staan, niet in staat om veel te bewegen.
Onthoud:
* De toestand van materie hangt af van temperatuur en druk. Een stof kan zijn status veranderen, afhankelijk van deze factoren.
* Er zijn uitzonderingen op deze generalisaties. Sommige vaste stoffen kunnen bijvoorbeeld behoorlijk samendrukbaar zijn en sommige vloeistoffen kunnen zeer lage dichtheden hebben.
 Als oplossing A een massa van 60 g en B 40 heeft wanneer ze gemengde chemische reactie zijn, wordt opgevoerd waarin gas wordt geproduceerd als het uiteindelijke mengsel 85 Welk produceren?
Als oplossing A een massa van 60 g en B 40 heeft wanneer ze gemengde chemische reactie zijn, wordt opgevoerd waarin gas wordt geproduceerd als het uiteindelijke mengsel 85 Welk produceren?  Hoeveel waterstofatomen zijn aanwezig in 2,32 mol C2H4?
Hoeveel waterstofatomen zijn aanwezig in 2,32 mol C2H4?  Is zwavel een elementverbinding of mengsel?
Is zwavel een elementverbinding of mengsel?  Wat zijn twee hoofdproducten van fotosynthese?
Wat zijn twee hoofdproducten van fotosynthese?  Heeft de atoombom de opwarming van de aarde opgezet?
Heeft de atoombom de opwarming van de aarde opgezet?
 De rol van microben in de productie van yoghurt
De rol van microben in de productie van yoghurt  Wat is een groot gebied bedekt met bomen gegroepeerd zodat hun gebladerte de grond in de grond schuilt?
Wat is een groot gebied bedekt met bomen gegroepeerd zodat hun gebladerte de grond in de grond schuilt?  Wat betekent opkomst in termen van de aardwetenschappen?
Wat betekent opkomst in termen van de aardwetenschappen?  Zelfs kleine hoeveelheden olie maakten vogels in de buurt van Deepwater Horizon ziek, onderzoekers zeggen:
Zelfs kleine hoeveelheden olie maakten vogels in de buurt van Deepwater Horizon ziek, onderzoekers zeggen: Rapport beveelt een nieuw raamwerk aan voor het schatten van de sociale kosten van koolstof
Rapport beveelt een nieuw raamwerk aan voor het schatten van de sociale kosten van koolstof
Hoofdlijnen
- Hoe verschilt de opperhuid van wortel van stam in structuur en functie?
- Welk wetenschapsgebied ontstond toen gerecombineerd DNA voor het eerst werd gemaakt in de
- Genetische ontdekking nog een hulpmiddel in de strijd tegen tarweplagen
- Wat zijn drie doelorganen van het parathyroïde hormoon?
- Wat osmose inhoudt. zowel water als zuurstof, maar niet noch noch zuurstof?
- Lijst voor- en nadelen van klonen op?
- Is een Meadow Mouse Carnivore?
- Wat is menselijk klonen?
- Wat is de functie van vetcel?
- Nieuwe biologische en veiligere zepen

- Lang gezochte structuur van telomerase effent de weg voor nieuwe geneesmiddelen voor veroudering, kanker
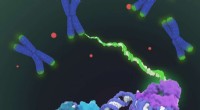
- Gerichte evolutie opent deur naar nieuwe antibiotica
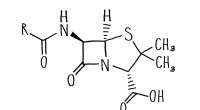
- Chemici tonen aan dat het katalytische bereik van enzymen kan worden vergroot
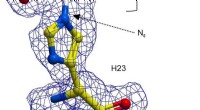
- Nieuwe technieken om de houdbaarheid van ons voedsel te verbeteren, kunnen het oogstverlies helpen minimaliseren

 Hoe beïnvloedt de dichtheid zoet water versus zout water?
Hoe beïnvloedt de dichtheid zoet water versus zout water?  De opwarming van de aarde kan de oorzaak zijn van een toename van de frequentie en intensiteit van koude periodes
De opwarming van de aarde kan de oorzaak zijn van een toename van de frequentie en intensiteit van koude periodes  Hoeveel centimeter om een 12 inch ronde bal te bedekken?
Hoeveel centimeter om een 12 inch ronde bal te bedekken?  Nanodeeltjes zoeken en vernietigen grondwatertoxines
Nanodeeltjes zoeken en vernietigen grondwatertoxines Wat betekent het woord satelliet in de wetenschap?
Wat betekent het woord satelliet in de wetenschap?  Oudere volwassenen kunnen gemeenschappen dienen als motoren van dagelijkse innovatie
Oudere volwassenen kunnen gemeenschappen dienen als motoren van dagelijkse innovatie Wat is de beste energiebron?
Wat is de beste energiebron?  Wie waren de Mercury 7?
Wie waren de Mercury 7?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

