
Wetenschap
Hoe verhoudt de dichtheid van een vloeistof zich met vaste stof?
* afstand van moleculen: In vaste stoffen zijn moleculen strak verpakt en gerangschikt in een gewone, rigide structuur. In vloeistoffen zijn moleculen losjes verpakt en kunnen ze bewegen, hoewel ze nog steeds dicht bij elkaar zijn.
* Compressibiliteit: Vaste stoffen zijn relatief niet -samendrukbaar, wat betekent dat je ze niet veel kunt persen. Vloeistoffen zijn meer samendrukbaar, waardoor hun moleculen onder druk dichter bij elkaar kunnen worden verpakt.
Uitzonderingen:
* Water: Water is een uitzondering, omdat de vaste vorm (ijs) minder dicht is dan zijn vloeibare vorm. Dit komt door de waterstofbruggen tussen watermoleculen die een meer open, kristallijne structuur in ijs creëren.
* Andere stoffen: Enkele andere stoffen, zoals bismut en silicium, hebben ook een hogere dichtheid in hun vloeibare vorm in vergelijking met hun vaste vorm.
Hier is een eenvoudige analogie:
Stel je een doos vol met knikkers voor (die moleculen vertegenwoordigen).
* solide: De knikkers zijn strak verpakt en bewegen niet veel.
* vloeistof: De knikkers kunnen zich bewegen, maar zijn nog steeds dicht bij elkaar.
De doos met de knikkers nauw opgepakt (vast) zou een hogere dichtheid hebben dan de doos met de knikkers losjes verpakt (vloeistof).
 Welke halogeenbroom of jodium zal de meer polaire binding vormen met fosfor?
Welke halogeenbroom of jodium zal de meer polaire binding vormen met fosfor?  Zou je verwachten dat sterke of zwakke zuren een lagere pH-waarde hebben?
Zou je verwachten dat sterke of zwakke zuren een lagere pH-waarde hebben?  Blijft een drankje kouder in een metalen blik of een plastic fles?
Blijft een drankje kouder in een metalen blik of een plastic fles?  Hoeveel mol zijn er in 85.636 gram koolstof?
Hoeveel mol zijn er in 85.636 gram koolstof?  Hoe ziet uranium er in zijn normale toestand uit?
Hoe ziet uranium er in zijn normale toestand uit?
Hoofdlijnen
- Waarom nucleïnezuren op een voedingslabel?
- Wat is bijvoorbeeld een regulerend voedsel?
- Hoe werden de nieuwe cellen gevormd uit de meiose vergeleken met elkaar?
- Wat is een goede superheldennaam voor mobiel?
- Wat zijn aanvullende genen?
- Een lastige zaak:hoe kankercellen somberder worden naarmate ze sterven
- Hoe wetenschappers de gezondheid van walvissen in de gaten houden door drones te gebruiken om hun slag op te vangen
- Wat is een soort voedsel dat het eet?
- Wat zijn de drie soorten klonen in eenvoudige vorm?
- De strijd tegen moeilijk te behandelen schimmelinfecties

- Chemici laten zien hoe vooringenomenheid kan opduiken in de resultaten van machine learning-algoritmen
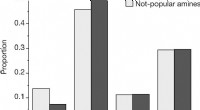
- Onderzoek naar nieuwe medicijnen kan de behoefte aan proefdieren drastisch verminderen
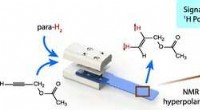
- Duurzamere mortels en beton met optimale thermische en mechanische efficiëntie

- Nieuw kathodemateriaal voor hoogwaardige natriumionbatterijen zou kunnen profiteren van grootschalige energieopslag

 Hoe lang duurt het voordat licht dat loodrecht op het glas valt, door deze 8,7 cm dikke sandwich gaat?
Hoe lang duurt het voordat licht dat loodrecht op het glas valt, door deze 8,7 cm dikke sandwich gaat?  Welk molecuul heeft de grootste gedeeltelijke negatieve lading chloride fluor broom jodiumkoolstof?
Welk molecuul heeft de grootste gedeeltelijke negatieve lading chloride fluor broom jodiumkoolstof?  Waarom is slechts een kleine hoeveelheid enzym nodig om de reactie te katalyseren met veel molecolen?
Waarom is slechts een kleine hoeveelheid enzym nodig om de reactie te katalyseren met veel molecolen?  Welk pad neemt lucht op de evenaar rond Hadley Convectiecel?
Welk pad neemt lucht op de evenaar rond Hadley Convectiecel?  Hoe is deeltjesbeweging gerelateerd aan materie?
Hoe is deeltjesbeweging gerelateerd aan materie?  Een zachte fototactische zwemrobot gebouwd met behulp van een zelfvoorzienende hydrogeloscillator
Een zachte fototactische zwemrobot gebouwd met behulp van een zelfvoorzienende hydrogeloscillator Hoe veranderde Bohrium Niels Bohr?
Hoe veranderde Bohrium Niels Bohr?  Welke fase van de celcyclus groeit een volledige grootte?
Welke fase van de celcyclus groeit een volledige grootte?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

