
Wetenschap
Welk molecuul heeft de grootste gedeeltelijke negatieve lading chloride fluor broom jodiumkoolstof?
* elektronegativiteit: Elektronegativiteit is het vermogen van een atoom om elektronen in een binding aan te trekken. Hoe hoger de elektronegativiteit, hoe sterker de trek op de gedeelde elektronen.
* Periodieke trends: Elektronegativiteit neemt toe naarmate je over een periode (van links naar rechts) beweegt en afneemt naarmate je een groep (boven naar beneden) op het periodiek systeem naar beneden beweegt.
Kijkend naar de lijst:
* chloor (CL), fluor (f), broom (br), jodium (i): Dit zijn allemaal halogenen en bevinden zich in dezelfde groep. Jodium staat onderaan de groep, wat betekent dat het de laagste elektronegativiteit heeft. Dit betekent dat jodium in een binding de zwakste aanleiding zal krijgen op gedeelde elektronen, wat resulteert in de grootste gedeeltelijke negatieve lading.
* koolstof (c): Koolstof is geen halogeen en heeft een lagere elektronegativiteit dan alle halogenen.
Daarom zal jodium de grootste gedeeltelijke negatieve lading hebben in vergelijking met de andere vermelde elementen.
Hoofdlijnen
- Wat zijn de drie theorieën voor het ontstaan van Homo Sapiens?
- Welke groep bevat het favoriete molecuul van de hersenen?
- In het moderne classificatiesysteem zijn drie domeinen?
- Hoe verschilt differentiatie in dier- en plantencel?
- Secretine-eiwit met een kroon
- Het unieke pentraxine-koolzuuranhydrase-eiwit reguleert het vermogen van vissen om te zwemmen
- Wat is het eindresultaat van bemesting in termen van chromosomen -getallen?
- Meeldauw versus schimmel:wat is het verschil?
- Wat is een pherorod?
- Atomaire vingerafdruk identificeert emissiebronnen van uranium

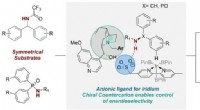
- Door metaal gekatalyseerde reacties die enantioselectief zijn gemaakt met behulp van chiraal kation
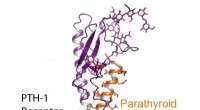
- Van receptorstructuur tot nieuwe osteoporosemedicijnen
- Gouddeeltjes gebruiken om het onzichtbare zichtbaar te maken

- Een nieuw natuurlijk blauw voor voedselkleuring

 Model geeft een duidelijker beeld van hoe zuurstof de atmosfeer van de aarde ging domineren
Model geeft een duidelijker beeld van hoe zuurstof de atmosfeer van de aarde ging domineren  Maak kennis met de odderon:Large Hadron Collider-experiment toont potentieel bewijs van quasideeltjes waarnaar al tientallen jaren wordt gezocht
Maak kennis met de odderon:Large Hadron Collider-experiment toont potentieel bewijs van quasideeltjes waarnaar al tientallen jaren wordt gezocht Wat is de empirische formule van aluminiumoxide?
Wat is de empirische formule van aluminiumoxide?  Hydrogel regelt de celgroei buiten het lichaam
Hydrogel regelt de celgroei buiten het lichaam Hoeveel is een bakje van een bowlingbal -formaat Jasper waard?
Hoeveel is een bakje van een bowlingbal -formaat Jasper waard?  Nieuwe mitochondriaal afgeleide peptiden laten zien wat ze kunnen doen
Nieuwe mitochondriaal afgeleide peptiden laten zien wat ze kunnen doen  Studie bepaalt burst-eigenschappen van de meest terugkerende transiënte magnetar
Studie bepaalt burst-eigenschappen van de meest terugkerende transiënte magnetar Ideeën voor een Math Field Trip
Ideeën voor een Math Field Trip
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


