
Wetenschap
Zou je verwachten dat sterke of zwakke zuren een lagere pH-waarde hebben?
pH is een maatstaf voor de zuurgraad of basiciteit van een oplossing. Het wordt gedefinieerd als de negatieve logaritme van de waterstofionenconcentratie in mol per liter. De pH-schaal varieert van 0 tot 14, waarbij 0 het meest zuur is en 14 het meest basisch.
Sterke zuren zijn zuren die volledig dissociëren in water, waarbij al hun waterstofionen vrijkomen. Dit resulteert in een hoge waterstofionenconcentratie en een lage pH. Zwakke zuren dissociëren daarentegen slechts gedeeltelijk in water, waarbij slechts een klein deel van hun waterstofionen vrijkomt. Dit resulteert in een lagere waterstofionenconcentratie en een hogere pH.
Zoutzuur (HCl) is bijvoorbeeld een sterk zuur dat volledig dissocieert in water, waarbij alle waterstofionen vrijkomen. Dit resulteert in een pH van 0. Azijnzuur (CH3COOH) is een zwak zuur dat slechts gedeeltelijk dissocieert in water, waarbij slechts een klein deel van de waterstofionen vrijkomt. Dit resulteert in een pH van 4,8.
 Impact van grote vulkaanuitbarstingen in de afgelopen twee millennia op zowel het mondiale als het Chinese klimaat
Impact van grote vulkaanuitbarstingen in de afgelopen twee millennia op zowel het mondiale als het Chinese klimaat  NASA vindt tropische storm Karens kracht aan de westkant
NASA vindt tropische storm Karens kracht aan de westkant Wijdverbreide adoptie van elektrische voertuigen zou miljarden dollars besparen, duizenden levens
Wijdverbreide adoptie van elektrische voertuigen zou miljarden dollars besparen, duizenden levens Wereldleiders komen samen om het akkoord van Parijs nieuw leven in te blazen
Wereldleiders komen samen om het akkoord van Parijs nieuw leven in te blazen Kent u de ecologische voetafdruk van uw voedselkeuzes?
Kent u de ecologische voetafdruk van uw voedselkeuzes?
Hoofdlijnen
- Hoe enzymen werken:UB-chemici publiceren een belangrijke ontdekking
- De functie van Peyers-patches
- Wat zijn de speciale dingen die gebeuren wanneer cellen worden gesplitst?
- Vogelneuronen gebruiken drie keer minder glucose dan zoogdierneuronen
- Hoe krijgt bloed zuurstof?
- Wat is hypothyreoïdie?
- Hoe schimmels voedingsstoffen beschikbaar maken voor de wereld
- De locatie van Cilia en Flagella
- Wijzigingen in de Amerikaanse importregels voor honden:wat ze zijn en waarom belangrijk voor hondenmensen
- Onderzoek onthult inzichten in enzym dat een algemeen broeikasgas bestrijdt

- C9h-peptide afgetopt om apoptose van kankercellen te induceren

- Nieuwe materialen van perovskiet dagen traditionele noties van hogedrukchemie uit

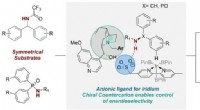
- Door metaal gekatalyseerde reacties die enantioselectief zijn gemaakt met behulp van chiraal kation
- Nieuw, volledig biologisch afbreekbaar cellulosemembraan blijkt effectief bij olie-waterscheiding

 Hoe een broeikaseffect te voorkomen
Hoe een broeikaseffect te voorkomen FlatScope:team ontwerpt lensvrije fluorescentiemicroscoop
FlatScope:team ontwerpt lensvrije fluorescentiemicroscoop De meeste elektrische voertuigen komen niet in aanmerking voor federale belastingvermindering
De meeste elektrische voertuigen komen niet in aanmerking voor federale belastingvermindering Wat zijn de componenten van de atoomstructuur?
Wat zijn de componenten van de atoomstructuur?  Als je over een aardbeving zou vliegen, zou je het vliegtuig dan voelen trillen?
Als je over een aardbeving zou vliegen, zou je het vliegtuig dan voelen trillen?  Hoe kinderen de basis van percentages aan te leren
Hoe kinderen de basis van percentages aan te leren  Antropoceen versus Meghalayan - waarom geologen strijden over de vraag of mensen een natuurkracht zijn?
Antropoceen versus Meghalayan - waarom geologen strijden over de vraag of mensen een natuurkracht zijn? Chemici testen het vermogen van Chemica om synthetische routes te genereren
Chemici testen het vermogen van Chemica om synthetische routes te genereren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

