
Wetenschap
Wie ontdekte dat elektronen in specifieke niveaus of schalen bewegen?
De ontdekking van elektronen die in specifieke niveaus of schalen bewegen, wordt toegeschreven aan niels bohr .
In 1913 stelde hij het Bohr -model voor voor van het atoom. Dit model verklaarde dat:
* Elektronen rond de kern in specifieke cirkelvormige paden genaamd energieniveaus of shells .
* Elk energieniveau heeft een vaste energie die eraan is gekoppeld.
* Elektronen kunnen tussen energieniveaus springen door fotonen van licht te absorberen of uit te stoten.
Dit model, hoewel niet helemaal nauwkeurig, was een belangrijke stap voorwaarts in het begrijpen van de atomaire structuur en legde de basis voor latere, meer geavanceerde modellen.
 Kaarten onthullen de waarheid over bevolkingsdichtheid in heel Europa
Kaarten onthullen de waarheid over bevolkingsdichtheid in heel Europa GPM vindt dat de regenval afneemt in extra-tropische storm Gabrielle
GPM vindt dat de regenval afneemt in extra-tropische storm Gabrielle Brandstofzuinige technologie kan het klimaat bedreigen, Volksgezondheid
Brandstofzuinige technologie kan het klimaat bedreigen, Volksgezondheid Het vermijden van plastic voor eenmalig gebruik werd normaal tot het coronavirus. Hier is hoe we kunnen terugkeren naar goede gewoonten
Het vermijden van plastic voor eenmalig gebruik werd normaal tot het coronavirus. Hier is hoe we kunnen terugkeren naar goede gewoonten Welke herbivoren zijn er in de regenbodem?
Welke herbivoren zijn er in de regenbodem?
Hoofdlijnen
- Research Paper Topics in Biochemistry
- Welke van de volgende is een meest voorkomende pathogene micro -organismen in Amerikaanse voedingsmiddelen?
- Wat is een fysieke beschrijving van amylase?
- Hoe kunnen de structuren van een plantencel als deels voedselketen functioneren?
- Hoe zijn termen genlocus en allel gerelateerd?
- Heeft een hybride allel er maar één voor eigenschap?
- Groep organismen die het minst op elkaar lijken?
- Waar is het skelet van een embryo hoofdzakelijk uit?
- Produceert bemesting van gameten een haploïde of diploïde cel?
- Ontdekking van natuurlijk chirale oppervlakken voor veiligere geneesmiddelen

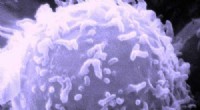
- Wetenschappers ontdekken verbinding die zich richt op kankercellen die het beschermende p53-voogdgen missen
- Wetenschappers ontdekken gemeenschappelijke blauwdruk voor eiwitantibiotica

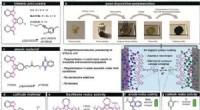
- Een volledig organische protonenbatterij die wordt geactiveerd voor duurzame energieopslag
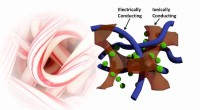
- Snoeprietpolymeerweefsel kan toekomstige functionele stoffen en apparaten van stroom voorzien
 Waarom een nieuwsgierige schaaldier het geheim zou kunnen houden om hernieuwbare energie uit hout te maken
Waarom een nieuwsgierige schaaldier het geheim zou kunnen houden om hernieuwbare energie uit hout te maken Wat is de juiste naam voor samengestelde HCL03?
Wat is de juiste naam voor samengestelde HCL03?  5 dingen die u niet wist over het metrische systeem
5 dingen die u niet wist over het metrische systeem  Artsen zeggen dat de meeste statistieken van uw Apple Watch, Fitbit is niet nuttig voor hen
Artsen zeggen dat de meeste statistieken van uw Apple Watch, Fitbit is niet nuttig voor hen Wat is de SI -eenheid voor de uiteindelijke snelheid?
Wat is de SI -eenheid voor de uiteindelijke snelheid?  Nieuwe tool haalt ongrijpbare COVID-19-marker uit menselijk bloed
Nieuwe tool haalt ongrijpbare COVID-19-marker uit menselijk bloed Faraday-stoffen? Met MXene gecoate stof kan elektronische interferentie in draagbare apparaten bevatten
Faraday-stoffen? Met MXene gecoate stof kan elektronische interferentie in draagbare apparaten bevatten Hoe verandert de elektrische kracht tussen twee geladen deeltjes als één lading wordt verminderd met een factor 3?
Hoe verandert de elektrische kracht tussen twee geladen deeltjes als één lading wordt verminderd met een factor 3?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

