
Wetenschap
Hoe verwijzen wetenschappers naar de potentiële energie binnen chemische bindingen?
Hier is een uitsplitsing:
* potentiële energie: Energie opgeslagen in een systeem vanwege zijn positie of configuratie.
* chemische bindingen: Krachten die atomen bij elkaar houden in moleculen.
bindingsenergie is de hoeveelheid energie die nodig is om een specifieke binding tussen twee atomen te verbreken, of de hoeveelheid energie die wordt vrijgegeven wanneer die binding wordt gevormd. Het is in wezen een maat voor de sterkte van de binding.
Hier zijn enkele belangrijke punten over bindingsenergie:
* eenheden: Bondsenergie wordt typisch gemeten in kilojoules per mol (kj/mol) of kilocalorieën per mol (kcal/mol) .
* typen: Bondsenergieën kunnen variëren, afhankelijk van de soorten atomen die betrokken zijn bij de binding en het type binding (enkele, dubbel, drievoudig).
* reacties: Bond -energieën spelen een cruciale rol bij het begrijpen van de energetica van chemische reacties. Wanneer bindingen worden verbroken, wordt energie geabsorbeerd en wanneer bindingen worden gevormd, wordt energie vrijgegeven. De algehele energieverandering van een reactie kan worden geschat door de bindingsenergieën van de reactanten en producten te overwegen.
Andere termen die u misschien ziet:
* Bond Enthalpy: Vergelijkbaar met bindingsenergie, maar meer specifiek verwijst naar de enthalpiewijziging die betrokken is bij het verbreken van een binding onder standaardomstandigheden.
* Bond dissociatie -energie: De energie die nodig is om een specifieke binding in een molecuul in de gasfase te verbreken.
Laat het me weten als je nog meer vragen hebt!
 Is het smeltend koper een exotherme proces?
Is het smeltend koper een exotherme proces?  Purdue drug discovery is gericht op het vinden van betere medicijnen, vermijd medicatietragedies zoals thalidomide
Purdue drug discovery is gericht op het vinden van betere medicijnen, vermijd medicatietragedies zoals thalidomide De toestand van materie vloeibare vaste stof of gas die een materiaal bestand is tegen compressie?
De toestand van materie vloeibare vaste stof of gas die een materiaal bestand is tegen compressie?  Hoe lang geleden was de vorming van basiselementen?
Hoe lang geleden was de vorming van basiselementen?  Het pad voor cellen verlichten
Het pad voor cellen verlichten
 Is het planten van bomen om de klimaatverandering tegen te gaan 'complete onzin'?
Is het planten van bomen om de klimaatverandering tegen te gaan 'complete onzin'?  Alaska vulkaan Q&A:uitbarstingen hebben hoogvliegende gevolgen
Alaska vulkaan Q&A:uitbarstingen hebben hoogvliegende gevolgen Hoe taal de temperatuur van het verhitte debat over klimaatverandering kan verlagen
Hoe taal de temperatuur van het verhitte debat over klimaatverandering kan verlagen  Getijden stabiliseren delta's totdat mensen tussenbeide komen
Getijden stabiliseren delta's totdat mensen tussenbeide komen Plaattektoniek legt de puzzel van de verschuivende aardkorst samen
Plaattektoniek legt de puzzel van de verschuivende aardkorst samen
Hoofdlijnen
- Is er moleculair bewijs voor evolutie?
- Hoe verlaten darmparasieten over het algemeen hun gastheer?
- Wat betekenen de bloedgroepletters?
- Voordelen en nadelen van Hydrostatic Skeleton
- Mechanische sensoren helpen de celorganisatie te coördineren tijdens oogontwikkeling
- Nieuwe experimenten bieden inzicht in hoe insecten vliegen en het ontwerpen van kleine vliegende robots
- Hoe beïnvloeden enzymen de reactiesnelheid?
- Zijn de bases van RNA a g c en u?
- Identieke cellen gevormd tijdens celdeling?
- Verlaging van de bedrijfstemperatuur van keramische brandstofcellen met een elektrolyt met hoge protongeleiding
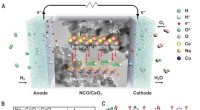
- Peilstoktechnologie kan een revolutie teweegbrengen in de diagnose van ziekten
- Fluorescerende techniek brengt verouderende polymeren aan het licht

- Enzymbiofabrieken om navelstrengbloedtransplantaties te verbeteren

- Bio-geïnspireerde op MXene gebaseerde actuatoren voor programmeerbare slimme apparaten
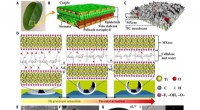
 Heeft een heliumatoom acht elektronen in zijn buitenste energieniveau?
Heeft een heliumatoom acht elektronen in zijn buitenste energieniveau?  Kan een nevel groter zijn dan ster?
Kan een nevel groter zijn dan ster?  Een vaste stof is 40 Newton wanneer het volledig wordt ondergedompeld in een vloeistof van relatieve dichtheid 0,8. het gewicht water berekenen?
Een vaste stof is 40 Newton wanneer het volledig wordt ondergedompeld in een vloeistof van relatieve dichtheid 0,8. het gewicht water berekenen?  Wat is het thema van de wetenschapsmaand 2012-2013?
Wat is het thema van de wetenschapsmaand 2012-2013?  Hoe worden natuurlijke selectie en evolutie gekoppeld?
Hoe worden natuurlijke selectie en evolutie gekoppeld?  Klimaatwip aan het einde van de laatste glaciale fase
Klimaatwip aan het einde van de laatste glaciale fase Hoe classificeren we micro -organismen?
Hoe classificeren we micro -organismen?  Nieuw onderzoek vindt dat transparantie van kosten de verkoop met 20% kan verhogen
Nieuw onderzoek vindt dat transparantie van kosten de verkoop met 20% kan verhogen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

