
Wetenschap
Kunnen de moleculen in de gasfase sneller bewegen dan dezelfde vloeibare fase?
* Kinetische energie en temperatuur: De gemiddelde kinetische energie van moleculen is recht evenredig met de absolute temperatuur. Hogere temperaturen betekenen hogere kinetische energie.
* staten van materie:
* gas: In de gasfase zijn moleculen ver uit elkaar en hebben ze zwakke intermoleculaire krachten (de aantrekkingskrachten tussen moleculen). Ze bewegen vrij en willekeurig, botsen tegen elkaar en de containerwanden.
* vloeistof: In de vloeibare fase zijn moleculen dichter bij elkaar dan in een gas. Ze bewegen nog steeds, maar hun beweging is beperkter vanwege sterkere intermoleculaire krachten.
* Energie vereist voor faseveranderingen: Er is energie voor nodig om over te stappen van een vloeistof naar een gas (verdamping). Deze energie verhoogt de kinetische energie van de moleculen, waardoor ze kunnen loskomen van het oppervlak van de vloeistof en de gasfase kunnen binnenkomen.
Samenvattend: Omdat gasmoleculen hogere kinetische energie hebben (vanwege zwakkere intermoleculaire krachten en typisch hogere temperaturen), bewegen ze sneller dan moleculen in de vloeibare fase.
Hoofdlijnen
- Red Tit-toxine stuurde hen naar het ziekenhuis. Kijk wat er gebeurde met een paar Florida-schildpadden
- Waarom zouden wetenschappers een hybride mens-koe-embryo willen creëren?
- Hoe reguleert Ph de ademhaling?
- Wat is het type eigenschap dat veel fenotypes heeft?
- Wat is het tweede trofische niveau in Food Web?
- Wat is het primaire mechanisme dat verantwoordelijk is voor evolutionaire verandering?
- Citeer omgevingsvariabele die de verdeling van levende organismen beïnvloedt?
- Waarom is wetenschappelijke modellen belangrijk?
- Update over bedreigde Filippijnse cycadsoorten
- Het aangaan van een 100 jaar oude uitdaging zou de weg kunnen banen naar digitale aroma's

- Onderzoekers ontwikkelen een nieuwe manier om een spectrum van natuurlijk ogende haarkleuren te creëren

- Nieuwe bacteriële testmethode om de gezondheidszorg te verbeteren, voedselveiligheid en meer
- Video:Kan Google u helpen de vlekken te verwijderen?

- Field-cycling relaxometrie kan de tumorstatus beoordelen door de snelheid van cellulaire wateruitwisseling te meten
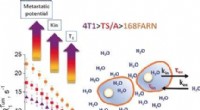
 Nieuwe Monte Carlo-code voor het oplossen van stralingsoverdrachtsvergelijkingen
Nieuwe Monte Carlo-code voor het oplossen van stralingsoverdrachtsvergelijkingen Studie volgt DACA's voordelen, beperkingen voor immigranten zonder papieren
Studie volgt DACA's voordelen, beperkingen voor immigranten zonder papieren Amplificatie en beeldvorming van microRNA als biomarker om tumorontwikkeling te detecteren
Amplificatie en beeldvorming van microRNA als biomarker om tumorontwikkeling te detecteren Wat produceert haploïde cellen?
Wat produceert haploïde cellen?  Welke beweging van de aarde zorgt ervoor dat de zon elke dag opkomt en ondergaat?
Welke beweging van de aarde zorgt ervoor dat de zon elke dag opkomt en ondergaat?  Het op lange termijn volgen van het voedselgedrag van walvissen via satelliet is nu mogelijk met nieuwe tag
Het op lange termijn volgen van het voedselgedrag van walvissen via satelliet is nu mogelijk met nieuwe tag Komen zwarte mannen in de stad tekort in de klas?
Komen zwarte mannen in de stad tekort in de klas?  Vodafone Egypte krijgt boete van 500, 000 euro voor dekking uitval
Vodafone Egypte krijgt boete van 500, 000 euro voor dekking uitval
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


