
Wetenschap
Welke twee regels van toepassing op elektronen?
1. Pauli Exclusion Principle: Dit principe stelt dat geen twee elektronen in een atoom dezelfde set van vier kwantumnummers kunnen hebben. Deze kwantumaantallen beschrijven het energieniveau van een elektron, de orbitale vorm, orbitale oriëntatie en spin. Dit betekent dat elk elektron in een atoom een unieke combinatie van deze eigenschappen moet hebben. Dit principe is cruciaal voor het begrijpen van de elektronische structuur van atomen en hoe ze chemische bindingen vormen.
2. Hund's regel: Deze regel stelt dat bij het invullen van orbitalen van gelijke energie (gedegenereerde orbitalen), elektronen elk orbitaal individueel bezetten voordat ze in een orbitaal worden verdubbeld. Bovendien zullen de elektronen in afzonderlijk bezette orbitalen dezelfde draai hebben. Dit betekent dat elektronen er de voorkeur aan geven zoveel mogelijk te verspreiden en parallelle spins binnen een subshell hebben. Deze regel helpt de stabiliteit van bepaalde elektronenconfiguraties te verklaren.
Deze regels zijn van fundamenteel belang om het gedrag van elektronen in atomen en moleculen te begrijpen.
Hoofdlijnen
- Is de celwand omgeven door een dubbel membraan en is de site voor fotosynthese in planten?
- Wat is insomina?
- Welk bioom bevindt zich in Canada en Rusland?
- Geurende reinigingsproducten: The New Smoking?
- De (blanco) gevonden in de nucleaire envelop zijn bekleed met gespecialiseerde eiwitten die het transport van stoffen in en uit de kern mogelijk maken?
- Wat is een actief proces waarmee het plasmamembraan een invagenatie kan vormen?
- Wat is een anti -codon?
- Waar bevindt de kern zich in plantencel?
- Wat wordt bedoeld met fenotype plasticiteit in wortels en scheuten?
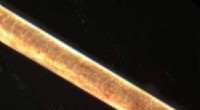
- Een nieuwe composiet voor treksterkte
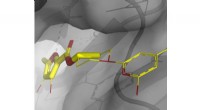
- Op fragmenten gebaseerde benaderingen gebruiken om nieuwe antibiotica te ontdekken
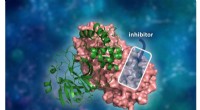
- Geschiedenis van inzichtelijk hiv-onderzoek inspireert neutronenverstrooiingsbenadering bij het bestuderen van COVID-19
- Oppervlaktemodificatie voor het verbeteren van de in vivo levensduur van bio-implantaten

- Betere en goedkopere zorg met droge bloedmonsters

 Afbeelding:uitzicht van een astronaut vanuit het kantoor op de hoek
Afbeelding:uitzicht van een astronaut vanuit het kantoor op de hoek Game review:Phoenix Point is chaotisch en heerlijk
Game review:Phoenix Point is chaotisch en heerlijk Wetenschappers versterken kwantumbouwstenen in mijlpaal die cruciaal is voor opschaling
Wetenschappers versterken kwantumbouwstenen in mijlpaal die cruciaal is voor opschaling Wat is een ecosysteem dat zowel zout water als zoet water bevat?
Wat is een ecosysteem dat zowel zout water als zoet water bevat?  Hoe mensen multiraciale gezichten waarnemen is niet altijd zo zwart-wit, zo blijkt uit onderzoek
Hoe mensen multiraciale gezichten waarnemen is niet altijd zo zwart-wit, zo blijkt uit onderzoek  Welke soorten energie worden opgeslagen in een parachute?
Welke soorten energie worden opgeslagen in een parachute?  Gezamenlijk onderzoek richt zich op de noodzaak voor het behoud van bronnen in een droog klimaat
Gezamenlijk onderzoek richt zich op de noodzaak voor het behoud van bronnen in een droog klimaat Welke winkels en lossen energie voor de cel uit?
Welke winkels en lossen energie voor de cel uit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


